Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химическое равновесие, закон действующих масс. Смещение равновесия, принцип ле – шателье. Уравнение химического сродства.Содержание книги
Поиск на нашем сайте
2. При 298 К энтропия ромбической серы Уравнение процесса: Sр ® Sм Вычисляем тепловой эффект этой реакции как разность энтальпий сгорания исходных веществ и продуктов. DHф.п. = DHсг(Sр) – DHсг(Sм) = –297,9 – (–298,2) = 0,3 кДж. Вычисляем изменение энтропии фазового перехода: DSф.п. = DHф.п. / T = 0,3 / 298 = 1,0·10–3 кДж/К. Рассчитываем энергию Гиббса: DGф.п. = DHф.п. – TDSф.п. = 0,3 – 298 · 1,0·10–3 = 0,002 кДж. DGф.п. > 0, поэтому переход Sр ® Sм при 298 К невозможен. Привести запись гальванического элемента, возникающего на посеребрённой стальной поверхности при нарушении целостности покрытия. Записать процессы коррозии во влажной атмосфере, указать продукты коррозии Запишем величины стандартных окислительно-восстановительных потенциалов металлов. E0(Fe2+/Fe) = –0,44 В E0(Ag+/Ag) = +0,80 В E0(Fe2+/Fe) < E0(Ag+/Ag), поэтому железо будет анодом, а серебро — катодом. Коррозия во влажном воздухе: катод: 2H2O + O2 + 4e– ® 4OH– (восстановление) анод: Fe0 – 2e– ® Fe2+ (окисление) Схема процесса: 2Fe + 2H2O + O2 = 2Fe(OH)2 На воздухе Fe(OH)2 подвергается дальнейшему окислению: 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 Таким образом, продукт коррозии — ржавчина Fe3O4, образуемая при высыхании гидроксидов железа. Схема гальванического элемента: (–) Fe | O2, H2O | Ag (+) Экзаменационный билет №11 Коллигативные свойства растворов не электролитов. Закон Рауля, явление осмоса, уравнение Вант – Гоффа
2. Термит Процесс восстановления металла из его оксида с помощью другого металла называется металлотермией. Если в качестве восстановителя применяется алюминий, то процесс называется алюминотермией. Применение термита основано на реакциях: Al0 – 3e– = Al+3 Fe3+ + 3e– = Fe0 Уравнение реакции: 2Al + Fe2O3 = Al2O3 + 2Fe Вычислим тепловой эффект этой реакции. DH0 = DH0(Al2O3) – DH0(Fe2O3) = –1676 – (–822,2) = –853,8 кДж. В 1 кг термита по условию содержится 75% алюминия (750 г) и 25% Fe2O3 (250 г). Вычислим количества веществ: n(Al) = m(Al) / M(Al) = 750 / 26,98 = 27,8 моль. n(Fe2O3) = m(Fe2O3) / M(Fe2O3) = 250 / 159,69 = 1,56 моль. Fe2O3 в недостатке, поэтому ведем расчет по нему. Q = –DH0 · n(Fe2O3) = 853,8 · 1,56 = 1331,9 кДж. При сгорании 1 кг термита выделится 1331,9 кДж теплоты. Рассчитать интервал значений энергии активации процессов, подчиняющихся правилу Вант-Гоффа, при изменении температуры от 300 К до 310 К Правило Вант-Гоффа — при повышении температуры на 10° скорость реакции увеличивается в 2-4 раза. Энергия активации связана с константами скорости процесса при двух температурах:
Известно, что отношение скоростей (и констант скоростей) при двух температурах связано с температурным коэффициентом скорости g:
Примем g = 2. По условию T2 – T1 = 310 – 300 = 10 К.
Примем g = 4.
Таким образом, интервал энергий активации 53594 … 107189 Дж. Экзаменационный билет №12
|
||||
|
Последнее изменение этой страницы: 2017-02-09; просмотров: 740; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.151 (0.006 с.) |

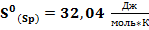 , а моноклинной
, а моноклинной  . Энтальпии сгорания соответственно равны:
. Энтальпии сгорания соответственно равны: 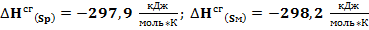 . Рассчитайте, возможно ли превращение
. Рассчитайте, возможно ли превращение 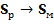 при
при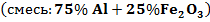 используется для термической сварки стальных изделий. Какое количество теплоты выделяется, если используется термит массой 1 кг?
используется для термической сварки стальных изделий. Какое количество теплоты выделяется, если используется термит массой 1 кг?
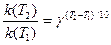
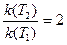
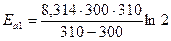 = 53594 Дж.
= 53594 Дж.
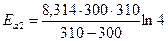 = 107189 Дж.
= 107189 Дж.