Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Набор заданий для проверки достижения конкретных целей обучения
Задание 1. Перемещение веществ в клетку осуществляется при помощи осмоса. Укажите, наличие каких двух факторов является причиной возникновения осмоса: A. Несмешивающиеся жидкости, разделенные ППМ; B. Растворы с одинаковой концентрацией, разделенные ППМ; C. Растворы с разной молярной концентрацией, разделенные ППМ; D. Растворы с разными несмешивающимися растворителями; E. Растворы, разделенные стеклянной перегородкой.
Задание 2. Явление гемолиза наблюдается в растворах определенной концентрации. Укажите процентное содержание раствора NaCl, в котором будет наблюдаться гемолиз. A. 12 B. 10 C. 5 D. 0,9 E. 0,1
Задание 3. Для расчета осмотического давления растворов электролитов вводится изотонический коэффициент i. Укажите фактора, который определяет величину данного коэффициента. A. Молекулярная масса вещества; B. Температура замерзания раствора; C. Природа растворителя; D. Степень диссоциации растворенного вещества; E. Осмотическое давление.
Задание 4. Вычислите осмотическое давление Концентрация раствора NaCl равна 0,1 моль/л при t° = 25°C (R = 0,082). Вычислите осмотическое давление данного раствора. A. 11,52; B. 6,73; C. 4,89; D. 1,29; E. 1,24.
Задание 5. Осмотическое давление одна из важнейших характеристик водных растворов. Укажите раствор с наибольшим осмотическим давлением. A. 0,1М глюкозы; B. 0,1М уксусной кислоты; C. 0,1М хлорида кальция; D. 0,1М хлорида натрия; E. 0,1М белка.
Задание 6. Раствор NaCl является изотоничным крови (Росм крови = 7,7 атм; R = 0,082). Укажите его молярную концентрацию. A. 0,41; B. 0,32; C. 0,25; D. 0,23; E. 0,15.
Задание 7. Гипертонические растворы солей MgSO4 и Nа2SO4 применяются в качестве слабительных средств. Укажите, какое уравнение можно использовать для расчета осмотического давления в растворе Nа2SO4. A. P = CRT; B. P = 2CRT; C. P = 3CRT; D. P = 4CRT; E. P = 5CRT.
Задание 8. Температура кипения раствора описывается следствием из закона Рауля. Укажите, как изменяется tкип физиологического раствора (0,9% раствора NaCl), если увеличить концентрацию соли в нем. A. Вначале повысится; B. Понизится, а потом понизится; C. Повысится; D. Не изменится; E. Повыситься или понизиться в зависимости от природы растворителя.
Эталоны ответов.
1 – C; 5 – C; 2 – E; 6 – E; 3 – D; 7 – C; 4 – C; 8 – C.
КРАТКИЕ МЕТОДИЧЕСКИЕ УКАЗАНИЯ К РАБОТЕ НА ПРАКТИЧЕСКОМ ЗАНЯТИИ.
Вначале занятия осуществляется проверка уровня подготовки студентов к занятию путем фронтальной беседы. После этого студенты решают ситуационные задачи по теме «Коллигативные свойства растворов». В процессе решения задач разбирается теоретический материал. Обращается особое внимание на медико-биологическое значение явления осмоса и применение растворов с различной осмотической концентрацией в клинической практике. Следующим этапом является проведение тестового контроля знаний по теме «Коллигативные свойства растворов» с использованием тестов формата А. Занятие заканчивается подведением итогов и объявлением результатов тестового контроля.
ОСМОС И ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ.
АКТУАЛЬНОСТЬ ТЕМЫ. Осмос имеет большое значение для растительных и животных организмов, способствуя оводнению клеток и межклеточных структур. Осмотическое давление обуславливает тургор клеток. Осмотическое давление плазмы крови человека характеризуется постоянством и равно 7,7 атм. Для возмещения больших потерь крови и при сильном обезвоживании внутривенно вводят физиологические растворы, изотоничные крови. Гипертоничные растворы применяются для обработки ран, при аллергических реакциях. В организме осмотическое давление является важным фактором, определяющим распределение воды и питательных веществ между органами и тканями. В медицинской практике используется криометрический метод определения осмотического давления по понижению температуры замерзания растворов.
ЦЕЛИ ОБУЧЕНИЯ. ОБЩАЯ ЦЕЛЬ. Уметь определять осмотическое давление растворов по депрессии температуры замерзания, а также рассчитывать осмотическую концентрацию растворов и молекулярную массу вещества.
КОНКРЕТНЫЕ ЦЕЛИ УМЕТЬ: 1. Определять депрессию температуры замерзания растворов. 2. Рассчитывать молярную, моляльную и массовую долю раствора. 3. Определять осмотическое давление растворов с помощью депрессии температуры замерзания этого раствора.
4. Рассчитывать молекулярную массу растворенного вещества. 5. Интерпретировать значение осмотического давления в биологии и медицине.
СОДЕРЖАНИЕ ОБУЧЕНИЯ. 1. ТЕОРЕТИЧЕСКИЕ ВОПРОСЫ. 1. Осмос. Осмотическое давление в растворах электролитов и неэлектролитов. 2. Осмотическое давление плазмы крови. Онкотическое давление. 3. Второй закон Рауля. Зависимость температуры замерзания и кипения от концентрации растворов и природы растворителя. 4. Криометрия и эбулиометрия и их использование в медико-биологических исследованиях. 5. Биологическая роль осмоса и осмотического давления в биологических системах.
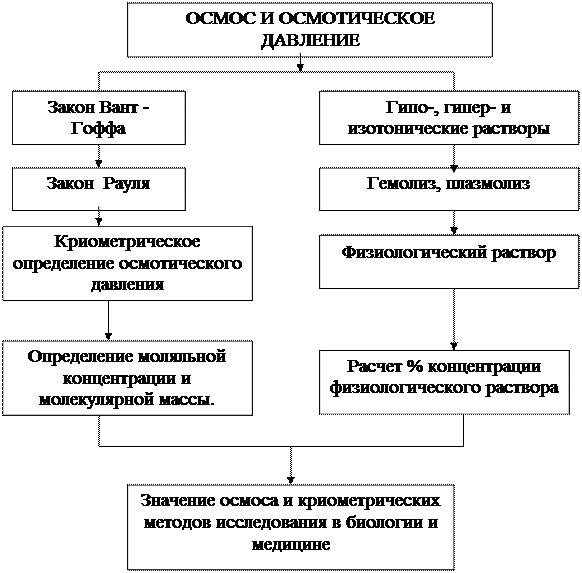
2. ГРАФ ЛОГИЧЕСКОЙ СТРУКТУРЫ ТЕМЫ.
3. ИСТОЧНИКИ ИНФОРМАЦИИ. Основная литература. 1. Мороз А.С., Луцевич Д.Д., Яворська Л.П. Медична хімія. – Вінниця: Нова книга, 2006. – С. 111-127. 2. Калибабчук В.А., Грищенко Л.И., Галинская В.И. и др. Медицинская химия: учебник. – К.: Медицина, 2008. – С. 126-141, 331-335. Дополнительная литература. 3. Л.П. Садовничая, В.Г. Хухрянский, А.Я. Цыганенко. Биофизическая химия. – К.: Вища шк. Головное изд-во, 1986. – С. 49-59. 4. Равич-Щербо М.И., Новиков В.В. Физическая и коллоидная химия. Учебник для ин-тов. – М.: Высш. школа, 1975. – С. 33-44.
|
|||||||||
|
Последнее изменение этой страницы: 2016-08-14; просмотров: 419; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.254.218 (0.013 с.) |