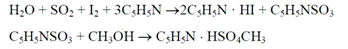Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Метод Къельдаля (обратное титрование).Содержание книги
Поиск на нашем сайте
Отличия от метода 1: выделившийся аммиак улавливают избытком титрованного раствора хлороводородной/серной кислоты, остаток кислоты титруют раствором натрия гидроксида в присутствии смешанного индикатора (из красно-фиолетовой в зеленую). Параллельно проводят контрольный опыт. NH3 + HCl → NH4Cl Избыток HCl + NaOH → NaCl + H2O Уравнения для расчета.
где: V 0 – объем 0,1 М раствора натрия гидроксида, израсходованный на титрование контрольного раствора, мл; V 1 – объем 0,1 М раствора натрия гидроксида, израсходованный на титрование испытуемого раствора, мл; K – поправочный коэффициент к титру раствора натрия гидроксида; Т – 1,401 мг/мл – титр 0,1М раствора гидроксида натрия по азоту; а – навеска образца лекарственного средства, г; Определение воды по К. Фишеру, значение метода для фармацевтического анализа. Преимущества, ограничения и разновидности метода. Состав реактива, химизм Взаимодействия с водой. Немногие органические реакции способны протекать в водной среде. Более того, вода способна оказывать разрушающее действие на многие органические соединения, приводить к побочным реакциям в химических процессах. Т.о. необходимо точное определение воды в используемых реагентах и/или растворителях. (по Фишеру определяется как гигроскопическая, так и кристаллизационная вода) Реактив К. Фишера представляет собой раствор серы диоксида, йода и пиридина в метаноле (должны быть безводными). Взаимодействие реактива с водой протекает в две стадии стехиометрически по уравнениям:
В качестве спирта обычно используется метанол, реже диэтиленгликоль. В качестве основания – пиридин, но чаще имидазол или первичные амины. Типы титрования по Фишеру Метод А Точную навеску испытуемого вещества, содержащую приблизительно от 30 до 50 мг воды, помещают в сосуд для титрования, в который предварительно внесено 5,0 мл метанола безводного. Титруют. КТТ по окраске титруемой жидкости (от желтой до красновато-коричневой) Параллельно проводят контрольный опыт (титруют 5,0 мл метанола безводного). Метод В Около 20 мл метанола безводного титруют реактивом К. Фишера, определяя конечную точку титрования амперометрически. Затем вносят точную навеску(по гф) испытуемого вещества. Титруют, определяя конечную точку титрования амперометрически. Метод С Около 10 мл метанола безводного титруют йодсернистым реактивом, определяя конечную точку титрования амперометрически. Затем быстро вносят точную навеску и точно отмеренный объем йодсернистого реактива, взятый с избытком приблизительно на 1 мл или объем, указанный в фармакопейной статье. Сосуд закрывают пробкой, выдерживают в защищенном от света месте в течение 1 мин или в течение времени, указанного в фармакопейной статье, периодически перемешивая содержимое сосуда. Избыток йодсернистого реактива титруют до первоначального значения силы тока, используя метанол безводный или растворитель, указанный в фармакопейной статье. Преимущества ● Высокая точность и воспроизводимость ● Селективность по воде ● Малые количества необходимых образцов ● Малое время анализа ● Практически неограниченный диапазон измерения (1ppm миллионная доля до 100 %) ● Пригоден для анализа: ○ Твердых веществ ○ Жидкостей ○ Газов Ограничения 1. Реагент Фишера неустойчив к действию света и влаги. Его стандартизация должна проводиться перед каждым использованием. 2. Рабочий интервал pH для определения воды по Фишеру между 5 и 8, в противном случае высоко кислотные или основные соединения рекомендуется буферизовать. 3. Плохо растворимые в метаноле соединения (например, жиры, углеводороды) следует растворять в высших спиртах или хлороформе, возможны также добавки формамида (для полярных веществ). 4. Следует избегать титрования веществ, которые способны реагировать с компонентами реактива Фишера (например, альдегиды и кетоны, сильные кислоты и основания, окислители и восстановители, соединения, реагирующие с компонентами реактива Фишера с образованием воды).
3. Определение азота аминокислот методами формольного и йодометрического
|
||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 183; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.115 (0.008 с.) |