Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Часть А. Дайте полное решение заданий. Укажите номер правильного ответа:
Укажите номер правильного ответа: 1. Электронная формула 1)
2. Пространственная конфигурация молекулы – линейная соответствует частицам (два варианта ответа): 1)
3. Тепловой эффект реакции: . 2РbS + 3О2 → 2РbО + 2SО2 ∆Н0обр КДж/Моль –94,28 0 −217,86 −296,9
1) ∆Нх.р.= − 840,96 КДж 3) ∆Нх.р.= + 420,00 КДж 2) ∆Нх.р.= + 840,96 КДж 4) ∆Нх.р.= − 420,00 КДж
4. Если энтальпия образования SO2 равна (− 297 КДж/моль), то количество теплоты, выделяемое при сгорании 16 г серы, равно ________________КДж 1) 74,25 2) 148,5 3) 297 4) 594
5. При проведении обратимой реакции 2СО (г) + О2 (г) ↔ 2СО2 (г) начальные концентрации СО и О2 были соответственно равны 0,8 и 0,5 моль/л, а в состоянии равновесия концентрация СО2 составила 0,2 моль/л, тогда константа равновесия равна _____________________________________ 1) 0,27 2) 4,56 3) 5,01 4) 6,03 Часть В. Выполните тестовые задания
Дополните: 1. Орбитальное квантовое число обозначается буквой __________, принимает значения _________________, характеризует ___________________________ 2. Свойства химических элементов изменяются периодически потому, что __ 3. В VII группе (главной подгруппе А) от астата к фтору радиус атома _____, энергия сродства к электрону ____, ОЭО ____, неметаллические свойства ____
4. 5. Число 6. Закон Гесса читается «Тепловой эффект химической реакции ___________ 7. Химическая реакция возможна, если ________________________________ 8. Закон действующих масс формулируется __________. Его математическое выражение имеет вид _______________________________________________
9. Константа химического равновесия характеризует _____________________ Укажите номер правильного ответа:
10. Четыре свободные 1)
11. Электронная формула иона 1)
12. Атому 1)
2)
13. Низшая степень окисления для элемента с электронной формой 1)
14. Вещества с ковалентной неполярной связью это: 1) кислород 3) цинк 2) хлороводород 4) аммиак 15. 1)
16. Оксид, легко разлагается при нагревании: 1) ½ О2 + Hg → HgO, ∆H= – 88,2 КДж/Моль 2) ½ О2 + Cu → CuО, ∆H= – 155 КДж/Моль 3) ½ О2 + Zn → ZnО, ∆H= – 357 КДж/Моль 4) ½ О2 + Mg → MgО, ∆H= – 600 КДж/Моль 17. У амфотерного (Al2O3) преобладают в большей степени свойства (подтвердите расчетами):
1) основные: Al2O3 + 3SO3 → Al2(SO4)3 ∆G0 КДж/Моль –1582 –370,0 –3094
2) кислотные: Al2O3 + CaO → Ca(AlO2)2 ∆G0 КДж/Моль –1582 –604,2 –2210 18. Если температурный коэффициент скорости химической реакции равен 3, то при повышении температуры от 10оС до 40оС скорость реакции _________ 1) увеличивается в 27 раз 3) увеличивается в 9 раз 2) уменьшается в 4 раза 4) уменьшается в 6 раз
19. Для смещения равновесия в системе 3Н2 (г) + N2 (г) ↔ 2NH3 (г) , ∆Н < 0 в сторону продуктов реакции необходимо ______________________________ 1) понизить концентрацию Н2 3) уменьшить давление 2) ввести катализатор 4) понизить температуру
20. При повышении давления в 2 раза скорость реакции 2SO2 (г) + О2 (г)→2SO3(г) увеличивается 1) в 4 разa 2) в 6 раз 3) в 8 раз 4) в 2 разa
ВАРИАНТ № 4
|
|||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 158; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.15.61.129 (0.008 с.) |
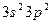 соответствует атому:
соответствует атому: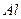 2)
2)  3)
3) 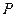 4)
4) 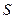
 2)
2) 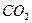 3)
3) 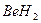 4)
4) 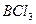
 - связь
- связь 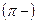 это связь – _________________________________________
это связь – _________________________________________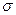 – связей в молекуле
– связей в молекуле 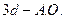 имеет атом:
имеет атом: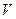 2)
2) 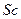 3)
3) 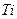 4)
4) 
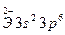 соответствует атому:
соответствует атому: 3)
3) 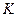 4)
4) 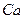
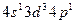 3)
3) 
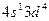 4)
4) 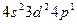
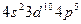 равна
равна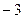 2)
2) 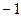 3)
3) 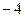 4)
4) 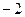
 - гибридизация в следующей частице:
- гибридизация в следующей частице: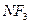 2)
2) 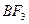 3)
3) 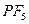 4)
4)