
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дисперсные системы и их классификация
В середине 19 века английский химик Томас Грэм (1805-1869) обнаружил вещества с загадочными свойствами. При выпаривании их растворов вместо кристаллов получались аморфные студенистые массы. Они имели клеющие свойства. По-гречески клей – «колла», поэтому Грэм назвал эти вещества коллоидами. Позже выяснилось, что из одного и того же вещества можно приготовить и обычный, и коллоидный раствор. Просто в обычных растворах вещество находится в виде отдельных молекул или ионов, а в коллоидных в виде крупных частиц. Например, поваренная соль в органическом растворителе (бензоле) образует типичную коллоидную систему. В любом коллоиде выделяются две фазы: сплошная (дисперсионная среда) и дисперсная или прерывистая – мелкие твердые частицы, капли жидкости или пузырьки газа. Крайне редки газы, жидкости или твердые материалы, в которых отсутствуют коллоидные частицы. Гелеобразную структуру имеет даже головной мозг. И. И. Жуков (представитель коллоидной химии) говорил, что «человек – ходячий коллоид». В зависимости от размера частиц дисперсные системы подразделяют на группы: а) взвеси (суспензии, эмульсии), у которых частицы имеют размер 10-6 м и более (1000 нм); б) коллоидные системы, размер частиц (от 10-9 м до Дисперсные системы также классифицируют по агрегатному состоянию дисперсной фазы и дисперсионной среды.
Коллоидные растворы. Коллоидное состояние характерно для многих веществ, если их частицы имеют размер от 1 до 500 нм (10-9 м Коллоидная частица имеет сложное строение. Она включает в себя: 1) ядро; 2) адсорбированные ионы; 3) противоионы; 4) растворитель. Примеры коллоидных частиц:
ядро
золь
ядро
золь
ядро
золь
Как видно, ядро состоит из электронейтрального агрегата с адсорбированными ионами элементов ( Коллоидная частица кроме ядра имеет противоионы и молекулы растворителя. Адсорбированные ионы и противоионы с растворителями образуют адсорбированный слой. Заряд коллоидной частицы равен разности зарядов адсорбированных ионов и противоионов. Вокруг частиц находится диффузный слой ионов, заряд которых равен заряду коллоидной частицы. Коллоидная частица и диффузный слой образуют электронейтральную мицеллу. Методы получения коллоидных растворов. Для приготовления коллоидных растворов следует получить частицы размером от 1 до 500 нм, подобрать дисперсионную среду, в которой не растворяется вещество частиц, обеспечить устойчивость частиц. Частицы соответствующих размеров получают: I. Дробление крупных частиц. Эти методы называются диспергационными. 1) механическое диспергирование (раздавливание, расщепление, истирание); 2) ультразвуковое диспергирование; 3) электрическое диспергирование. II. Объединение молекул или ионов. Такие методы называются конденсационными. 1) конденсация из паров при понижении температуры; 2) метод замены растворителя – дисперсионная фаза возникает вследствие меньшей растворимости вещества в новом растворителе. 3) химические методы (дисперсионная фаза возникает в результате ОВР, гидролиза или реакции обмена. Например, в результате гидролиза солей железа (III) получают его гидроксид: В качестве вещества коллоидных частиц в водных средах служат металлы, оксиды, гидрокисды, сульфиды и другие. Для повышения устойчивости коллоидов в раствор вводят стабилизаторы, например, ПАВ или ионы вещества, из которого состоит частица.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 59; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.139.79.46 (0.007 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
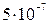 м) от 1 до 500 нм.
м) от 1 до 500 нм.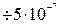 м).
м).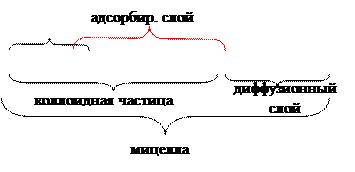
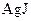
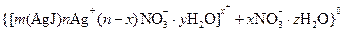
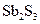

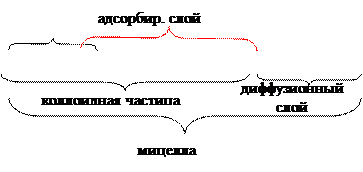
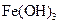
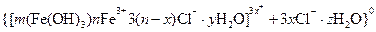
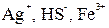 ).
). ).
).


