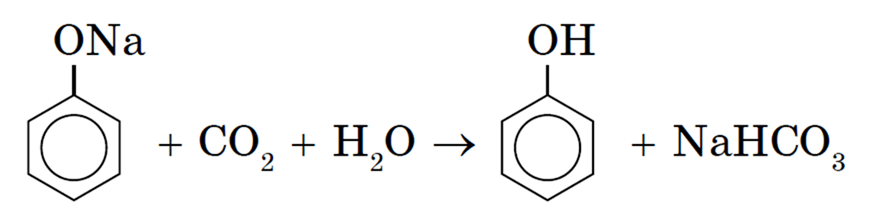Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
I Реакции с участием гидроксильной группы.
Неподеленная электронная пара кислорода вступает в сопряжение с p-электронной системой бензольного кольца, поэтому в фенолах полярность связи –О–Н увеличена:
Фенолы – более сильные кислоты, чем спирты, поэтому раньше фенол называли карболовой кислотой. 1) В растворе фенол диссоциирует с образованием Н+:
В растворе фенола (в отличии от растворов спиртов) индикаторы меняют свой цвет, показывая кислую среду. Но фенол – слабая кислота, слабее даже угольной. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей. Но если в бензольное кольцо ввести электронноакцепторный заместитель, полярность связи –О–Н увеличится, например популярное соединение 2,4,6-тринитрофенол (пикриновая кислота) сильнее угольной:
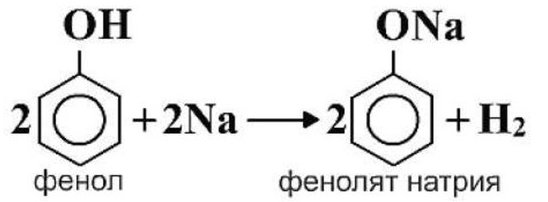
2) Как и спирты, фенол реагирует со щелочными металлами с образованием фенолятов:
см. опыт: https://youtu.be/XULMmtL5j7I
Любая кислота, даже раствор СО2, вытесняет фенол из фенолята:
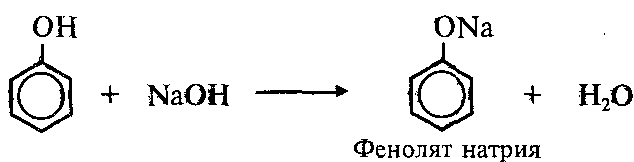
3) В отличии от одноатомных спиртов, фенол, являясь более сильной кислотой, реагируют с растворами щелочей:
см. опыт: https://youtu.be/A7kFugtDKR8
4) Качественная реакция на фенол – реакция с солями железа(III): образуется фенолят железа, раствор окрашивается в фиолетовый цвет:
фенолят железа см. видео: https://youtu.be/78MleZfhQNE
5) В отличии от спиртов, фенол не реагирует с галогенводородными кислотами (спирты реагируют с НГ).
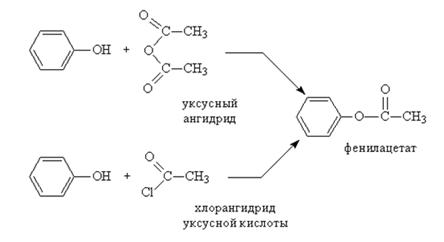
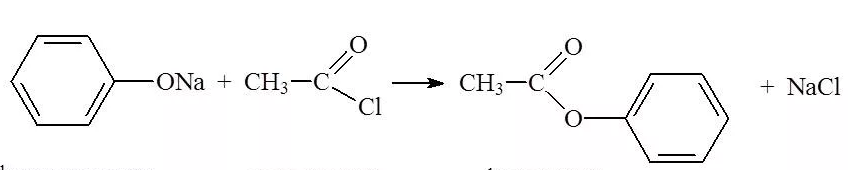
6)!!! В отличии от спиртов, фенол непосредственно не реагирует с карбоновыми кислотами (спирты реагируют с карбоновыми кислотами с образованием сложных эфиров). Сложные эфиры фенола можно получить при взаимодействии фенола с ангидридами или галогенангидридами кислот, например:
или через фенолят натрия:
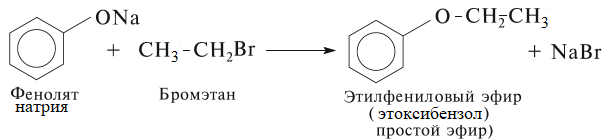
7) Простые эфиры образуются при взаимодействии фенола с галогеналканами, например:
8) Фенолы вступают в реакцию с альдегидами, наиболее известна реакция поликонденсации фенола с формальдегидом – образование фенол-формальдегидных смол (см. свойства альдегидов). см. видео https://youtu.be/WlNMzWGqb_U
II Реакции с участием бензольного кольца. Группа –ОН – электродонорный заместитель, ориентант I рода, она повышает электронную плотность в бензольном кольце, особенно в орто- и пара-положениях, поэтому:
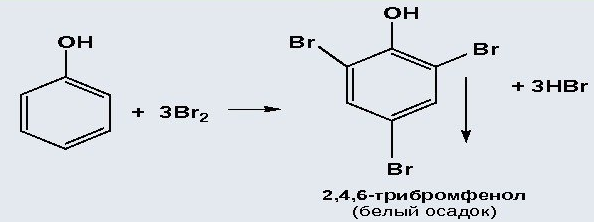
фенол значительно активнее бензола вступает в реакции электрофильного замещения 1)!!! В отличие от бензола, фенол реагирует с бромной водой. Это одна из качественных реакций на фенол: бромная вода обесцвечивается, выпадает белый осадок 2,4,6-трибромфенола:
см. опыт https://youtu.be/DwpuWDbBdho
|
|||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 96; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.51.55 (0.005 с.) |


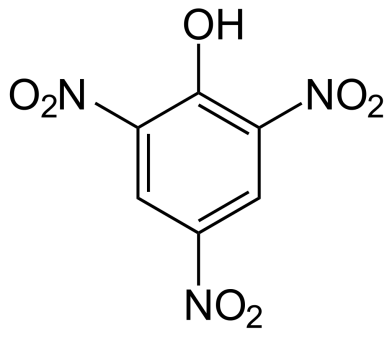 пикриновая кислота
пикриновая кислота