Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Работа № 10. Определение ЭДС элемента Якоби-ДаниэляСодержание книги
Поиск на нашем сайте Цель работы – изучение устройства и принципа действия гальванических элементов − химических источников тока (ХИТ). Знакомство с методом измерения электродных потенциалов и электрохимических характеристик ХИТ. Изучение зависимости потенциалов электродов первого рода от концентрации катиона и измерение ЭДС элемента Якоби-Даниэля. Использование результатов электрохимических измерений для расчета термодинамических параметров реакций. Оборудование
1. рН-метр (рН-340) − высокоомный вольтметр для измерения ЭДС. 2. Хлорсеребряный электрод сравнения. 3. Химические стаканы для растворов солей разных концентраций. 4. Электролитический ключ − U-образная стеклянная трубка, заполненная КСl и агар-агаром для увеличения вязкости раствора. 5. Медный и цинковый электроды. Последовательность выполнения работы 1. Включить рН-метр для прогревания на 10−15 мин. 2. В три стакана налить 1 М; 0,1 М и 0,01 М растворы соли цинка. 3. Составить гальванический элемент из цинкового и хлорсеребряного электрода сравнения (Ag, AgС1|КС1нас), для чего погрузить цинковый электрод в первый из трёх стаканов, соединить U-образной трубкой электролиты обоих электродов и подсоединить их к рН-метру. 4. Замерить разность потенциалов данного гальванического элемента. Показания снимать по верхней шкале прибора (описание прибора прилагается). 5. Построить гальванические элементы из цинкового электрода с другими концентрациями соли и хлорсеребряного электрода и замерить их разность потенциалов. 6. Такие же измерения провести с медным электродом, помещенным в растворы медной соли с разной ее концентрацией и хлорсеребряным электродом.
7. Составить гальванический элемент из цинкового и медного электродов с 1 М растворами соответствующих электролитов (гальванический элемент Якоби-Даниэля), соединив растворы электролитическим ключом, и замерить разность потенциалов элемента при комнатной температуре.
На основании полученных данных
1. Рассчитать потенциалы (Еоп) цинковых и медных электродов. При этом иметь в виду, что так как потенциал медного электрода более положителен, чем потенциал хлорсеребряного электрода, величина которого при 20°С составляет величину Ех-с = 0,201В, то измеренная в опыте разность потенциалов 2. По формуле Нернста, используя табличные значения стандартных потенциалов медного и цинкового электродов, рассчитать теоретические значения потенциалов Етеор для электродов с разными концентрациями солей цинка и меди. 3. Рассчитать ЭДС элемента Якоби-Даниэля и сравнить ее с опытным значением измеренной разности потенциалов. 4. Полученные данные записать в таблицу и рассчитать % ошибки опытных результатов по сравнению с теоретическими.
5. Рассчитать ∆G0 реакции. КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ 1. Опишите механизм возникновения электродных потенциалов металлов. При каких условиях электродный потенциал называется стандартным (или нормальным)? Приведите формулу Нернста для расчетов потенциалов электродов 1-го и 2-го рода. 2. Рассчитайте величину электродного потенциала железа, погруженного в 0,01 М раствор соли FeS04, если кажущаяся степень диссоциации равна 40%. 3. Какова схема гальванического элемента, в котором протекает реакция Cu + 2Ag+ = Сu+2 + 2Ag? Рассчитайте ЭДС этого элемента и величину ∆G0. 4. Какие процессы происходят на электродах в гальваническом элементе: (-} Mg|Mg(NO3)2||AgNO3|Ag (+)? Определите ЭДС этого элемента.
|
|||||||
|
Последнее изменение этой страницы: 2021-03-10; просмотров: 474; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.41 (0.008 с.) |

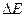 = ЕСu - Ех-с.. Для цинкового электрода:
= ЕСu - Ех-с.. Для цинкового электрода: 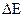 = Ех-с – ЕZn.
= Ех-с – ЕZn.