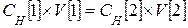Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Раствор состоит из растворенных веществ и растворителя.Содержание книги
Поиск на нашем сайте Растворитель – компонент, который преобладает и находится в том же агрегатном состоянии, что и раствор. Истинные и коллоидные растворы В растворах вещества могут находиться в различных степенях дисперсности (т.е. раздробленности). Величина частиц служит важным признаком, обуславливающим многие физикохимические свойства растворов.
По величине частиц растворы делятся на: 1. Истинные растворы (размер частиц меньше 1 мкм) и 2. Коллоидные растворы (размер частиц от 1 до 100 мкм).
Смеси с частицами размером более 100 мкм образуют взвеси: суспензии и эмульсии.
Истинные растворы могут быть ионными или молекулярными в зависимости от того, диссоциирует ли растворённое вещество на ионы или остаётся в недиссоциированном состоянии в виде молекул.
Коллоидные растворы резко отличаются по свойствам от истинных растворов. Они гетерогенны, так как имеют поверхность раздела между фазами – растворённым веществом (дисперсной фазой) и растворителем (дисперсионной средой). В процессе растворения частицы (ионы или молекулы) растворяемого вещества под действием хаотически движущихся частиц растворителя переходят в раствор, образуя в результате беспорядочного движения частиц качественно новую однородную систему. Процесс растворения является обратимым, так как может осуществляться не только переход частиц растворяемого вещества в раствор, но и выделение частиц из раствора в результате, например, процесса кристаллизации. Через определенное время процессы растворения или выделения частиц при данных внешних условиях приводят систему к состоянию равновесия – состоянию, в котором скорости этих процессов равны. В состоянии равновесия образуются насыщенные растворы. Насыщенным раствором называется такой раствор, который находится в равновесии с избытком растворяемого вещества – он содержит максимально возможное при данных условиях количество растворенного вещества. Если скорость растворения превышает скорость выделения, то образуются ненасыщенные растворы, если наоборот – пересыщенные. По соотношению количеств растворенного вещества и растворителя растворы подразделяют на разбавленные и концентрированные ( растворы, близкие к состоянию насыщения ). Концентрация насыщенного раствора для данного вещества при строго определенных условиях (Т, Р и растворитель) – величина постоянная и называется растворимостью вещества. Растворимость – способность вещества растворятся в растворителе. Количественной характеристикой растворимости является коэффициент растворимости. Он показывает, какая максимальная масса вещества может растворится в 1000 мл (т.е. 1 литре) растворителя при данной температуре. Растворимость выражается в г/л. По растворимости в воде вещества делятся на три группы: 1. Хорошо растворимые (в таблице растворимости обозначаются буквой «р») более 10г вещества в 1 л воды при температуре 20оС (сахар в воде); 2. Малорастворимые – «м» 0,01 – 10г на 1л воды (сульфат кальция – гипс в воде); 3. Практически нерастворимые – «н» менее 0,01 г. Растворимость зависит от природы растворителя, природы растворенного вещества, температуры и давления для газов. Так растворимость газов при повышении температуры уменьшается, а при увеличении давления увеличивается. Растворимость же многих твердых веществ при нагревании увеличивается. Зависимость растворимости от температуры показывают кривые растворимости. По ним можно определить: коэффициент растворимости веществ при различных температурах и массу растворенного вещества, которая выпадает в осадок при охлаждении раствора. Количественной характеристикой растворимости является концентрация. Концентрацией раствора называется количество растворенного вещества, содержащегося в определенном количестве раствора или растворителя. Концентрацию раствора можно выражать по разному. 2. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ Массовая концентрация, массовая доля w– отношение массы растворенного вещества m [ X ] к массе всего раствора m [ S ]
Массовая доля выражается в долях единицы или процентах. Пример. 5%-ный раствор серной кислоты в 100 граммах раствора содержит 5 грамм H2SO4 и 95 грамм растворителя – воды. Молярная концентрация, молярность СМ (М) – число молей растворенного вещества n [ X ], содержащегося в 1 л раствора V [ S ]
Различают обозначения: 0,1М – децимолярный; 0,01М – сантимолярный (0,02М – двусантимолярный); 0,001М – милимолярный. Пример. 1,5М раствор H2SO4 или СМ = 1,5 моль/л H2SO4 В 1000 мл раствора содержится 1,5 моля серной кислоты или в 1 л раствора содержится 1,5 ´ 98 = 147 г, где 98 – молярная масса серной кислоты. Для пересчета молей в граммы используем молярную массу вещества. Пример. Определите массу нитрата натрия, которая требуется для приготовления 2 л децимолярного раствора.
В 1 л раствора содержится СМ ´ М [ X ] = 0,1 ´ 85 = 8,5 г NaNO3 Составим пропорцию: в 1 л раствора содержится 8,5 г NaNO3 в 2 л раствора содержится х г NaNO3 Тогда х = 17 г нужно взять, чтобы приготовить 2 л 0,1М раствора. Эквивалентная концентрация, нормальность C Н - число эквивалентов растворенного вещества n Е, содержащихся в 1 л раствора V [ S ]
Различают обозначения: 0,1н – децинормальный; 0,01н – сантинормальный; 0,001н – милинормальный. Если в растворе содержится 1 эквивалент вещества, то это 1н раствор. Один эквивалент весит эквивалентную массу. Пример. 0,75н раствор H2SO4 или C Н = 0,75 моль/л H2SO4 В 1000 мл раствора содержится 0,75 моль серной кислоты или в 1 л раствора содержится 0,75 ´ 49 = 36,75 г, где 49 – эквивалентная масса серной кислоты. В общем виде: в 1 л раствора содержится СН ´ МЭ [ X ] в заданном V [ S ] раствора содержится х г Моляльная концентрация, моляльность Cm – число молей растворенного вещества n [ X ], приходящихся на 1 кг растворителя mP
Пример. 2m раствор H2SO4 2 моля приходятся на 1000 г растворителя (т.е. воды) Cm ´ М [ X ] приходятся на 1000 г растворителя Титр Т – показывает количество граммов растворенного вещества m [ X ], содержащихся в 1 мл раствора V [ S ]
Пример. Титр раствора равен 0,0036 г/мл. Это значит, что в 1 мл раствора содержится 0,0036г растворенного вещества. Если растворы имеют разную нормальность, то применяют: Закон эквивалентов для растворов
Объемы реагирующих веществ обратно пропорциональны их нормальностям.
|
||
|
Последнее изменение этой страницы: 2020-11-11; просмотров: 126; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.006 с.) |

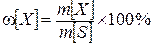
 [ моль / л; моль / см 3]
[ моль / л; моль / см 3]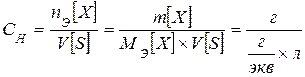 [ экв / л; моль / л ]
[ экв / л; моль / л ] [ моль / кг ]
[ моль / кг ] [ г/мл ]
[ г/мл ]