Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Лабораторная работа № 9. Расчет горения органического топливаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Цель работы: определение расхода окислителя и выхода продуктов полного сгорания органического топлива; определение энтальпии и влагосодержания
Основные понятия Существует два метода расчета горения органического топлива. Первый метод осуществляют по данным состава топлива, задаваясь коэффициентом избытка воздуха. Второй метод осуществляется по данным газового анализа с учетом состава сжигаемого топлива. Первый метод расчета применяется при проектировании топливоиспользующих установок, второй – при теплотехнических испытаниях, наладке оптимального процесса сжигания топлива в печах и топках. Материальный и тепловой балансы процесса горения проводят на 1м3 газообразного топлива и на 1 кг твердого или жидкого топлива. Состав газового топлива приводится по компонентам химических соединений в процентах от их объема, а для твердого и жидкого топлива приводится элементарный химический состав в процентах от их массы. Топливо в том виде, в каком оно поступает к потребителю, называется рабочим, а вещество, составляющее его, – рабочей массой. В элементарный химический состав его, выражаемый следующим образом:
CP+HP+OP+NP+SP+AP+WP=100 %,
входят горючие вещества – углерод S, водород S, а так же кислород O и азот N, находящиеся в сложных высокомолекулярных соединениях. Топливо содержит влагу W и негорючие минеральные примеси, превращающиеся при сжигании топлива в золу A. Минеральные примеси и влажность одного и того же сорта топлива в разных районах его месторождения могут быть разными, поэтому в справочной литературе приводится более постоянный состав горючей массы топлива, который используется для сравнительной теплотехнической оценки различных сортов топлива. Пользуясь пересчетным коэффициентом Расход кислорода и количество образующихся продуктов сгорания определяются из стехиометрических уравнений горения. Количество воздуха для горения топлива подается в топку больше его теоретически необходимого количества. Отношение количества воздуха, действительно поступившего в топку V в к теоретически необходимому Для вновь проектируемых топливоиспользующих установок величину α выбирают в зависимости от вида сжигаемого топлива, метода сжигания и конструкции топки. Для пылеугольных топок по условиям достижения большего значения КПД и интенсификации процесса горения оптимальными являются α=1,2 – 1,25, при этом нижний предел относится к бурым и каменным углям, а верхний – к тощим углям и антрацитам. При сжигании природных газов и мазута в агрегатах, снабженных автоматикой горения и регуляторами давления в газопроводе, α может быть снижен до 1,05. Расход топлива в топливоиспользующей установке данной производительности зависит от теплоты его сгорания, которая для различных видов топлив изменяется в больших пределах. При отсутствии опытных и справочных данных для приближенного расчета низшей теплоты сгорания твердого и жидкого топлива в МДж/кг:
в которой коэффициенты подобраны экспериментально и несколько отличаются от теплоты сгорания отдельных горючих элементов, входящих в состав топлива. Для сравнения по энергетической ценности и эффективности использования различных сортов топлив введено понятие об условном топливе, которому присваивается теплота сгорания, равная Qусл = 29,33 МДж/кг (7000 ккал/кг). Пересчет расхода данного топлива В в условное производится по соотношению Понятием условного топлива пользуются также при планировании добычи и потреблении топлива.
Порядок выполнения работы. Расчет расход окислителя и выход продуктов полного сгорания газообразного топлива. Объем кислорода, необходимого для сгорания газообразного топлива и образующихся продуктов сгорания подсчитывают на основе уравнения горения компонентов, входящих в состав газообразного топлива
Окись углерода CO+0,5O2+1,88N2=CO2+1,88N2 Водород H2+0,5O2+1,88N2=H2O+1,88N2 Метан CH4+2O2+7,52N2=CO2+2H2O+7,52N2 Этан C2H6+3,5O2+13,16N2=2CO2+3H2O+13,16N2 Пропан C3H8+5O2+18,8N2=3CO2+4H2O+18,8N2 Бутан C4H10+6,6O2+24,44N2=CO2+5H2O+24,44N2 Пентан C5H12+8O2+30,08N2=5CO2+6H2O+30,08N2 В соответствии с приведенными выше уравнениями горения компонентов газового топлива объем кислорода, необходимого для сгорания 1м3 газа, подсчитывают по формуле, м3/м3 газа
Объем воздуха Действительное количество воздуха подаваемое в топку, м3/м3 газа: где α – коэффициент избытка воздуха. Суммарный объем продуктов полного сгорания Объем продуктов сгорания за вычетом объема водяных паров называется объемом сухих газов: Выход двуокиси углерода, м3/м3 газа Выход азота складывается из азота воздуха, подаваемого в топку, и азота, содержащегося в газовом топливе, м3/м3 газа Выход водяных паров определяется с учетом содержания водорода и влаги в топливе – d м3/м3 газа и водяных паров, содержащихся в воздухе, используемом в качестве окислителя. Содержание в воздухе водяных паров принимают около 1 % по массе (1,6 % по объему), так как влагосодержание воздуха dв=10…16 г/м3 сухого воздуха при относительной влажности Выход водяных паров при сжигании газового топлива, м3/м3 газа:
Количество кислорода в продуктах сгорания, м3/м3 газа Расчет расхода окислителя и выхода продуктов полного сгорания твердого и жидкого топлива. Количество кислорода воздуха Oв, необходимое для полного сгорания 1 кг топлива, кг/кг где CP, SP, HP и OP – соответственно содержание углерода, горючей серы, водорода и кислорода в рабочей массе топлива в процентах по массе. Количество сухого воздуха Объем воздуха, теоретически необходимый для сгорания 1 кг топлива, равен или округленно, м3/кг Суммарный объем продуктов сгорания
объем двуокиси углерода, м3/кг Объем двуокиси серы, м3/кг Объем азота, м3/кг Объем водяного пара в продуктах сгорания с учетом содержания в воздухе около 1% влаги по массе (1,6% по объему), м3/кг Объем кислорода, м3/кг Для теплотехнических расчетов топок, теплогенераторов и других теплотехнологических установок необходимо знать энтальпию и влагосодержание продуктов сгорания топлива. Энтальпия влажных топочных газов отнесенная к массе сухих газов, кДж/кг где Масса сухих газов, кг где Влагосодержание топочных газов отнесенное к массе сухих газов, кг/кг где
Контрольные вопросы Что называется топливом? Что называется теплотворной способностью топлива? Чем отличается высшая теплота сгорания от низшей? Что называется условным топливом и для чего ввели данное понятие? Что называется балластом топлива и как он влияет на теплотворную способность топлива? Что называется коэффициентом избытка воздуха и как он влияет на эффективность использования топлива? Какие составляющие элементы топлива обуславливают его теплотворную способность? Расскажите о стадиях горения твердого топлива. Особенности горения жидкого топлива. Приложения
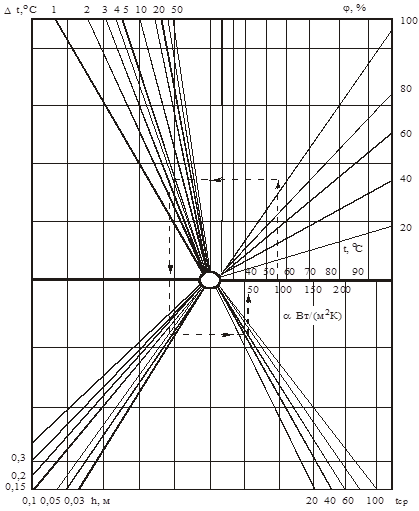
Приложение 1 Номограмма для определения коэффициента теплообмена от паровоздушной смеси к сплошным железобетонным изделиям при конденсации и естественной конвекции
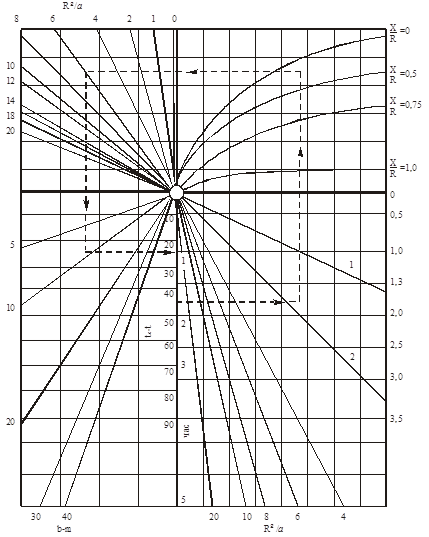
Приложение 2 Номограмма для определения температуры и времени нагрева железо- бетонных изделий при изменении температуры паровоздушной среды по линейному закону
Приложение 3 Приложение 4
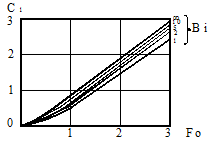
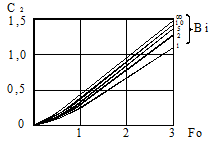
Кривые С1= f (Fo, Bi) для шара Кривые С2= f (Fo, Bi) для шара
Приложение 5
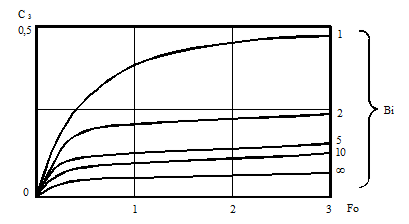
Кривые С3= f 3 (Fo, Bi) для шара
Приложение 6 Теплофизические характеристики материалов
Приложение 7
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 552; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.41 (0.007 с.) |

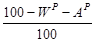 , определяют величину составляющих элементов рабочей массы по величине составляющих элементов в горючей массе.
, определяют величину составляющих элементов рабочей массы по величине составляющих элементов в горючей массе.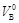 называют коэффициентом избытка воздуха
называют коэффициентом избытка воздуха 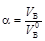 .
.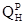 = 0,339СP+1,03HP– 0,109(OP–SP) – 0,0251WP,
= 0,339СP+1,03HP– 0,109(OP–SP) – 0,0251WP,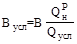 .
.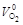 = 0,01(0,5CO+0,5H2+2СН4+3,5С2Н6+5С3Н8+6,5С4Н10+8С5Н12–О2)
= 0,01(0,5CO+0,5H2+2СН4+3,5С2Н6+5С3Н8+6,5С4Н10+8С5Н12–О2)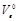 , необходимый для сгорания 1м3 газового топлива в стехиометрических условиях, подсчитывают исходя из содержания в воздухе 21% кислорода по объему, м3/м3 газа
, необходимый для сгорания 1м3 газового топлива в стехиометрических условиях, подсчитывают исходя из содержания в воздухе 21% кислорода по объему, м3/м3 газа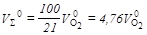 .
.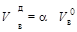
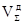 , состоящий из следующих компонентов, м3/м3 газа
, состоящий из следующих компонентов, м3/м3 газа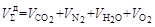 .
.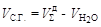
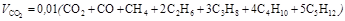
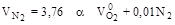 .
.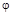 =50…60 % и температуре t=20…30 оС.
=50…60 % и температуре t=20…30 оС.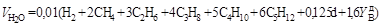
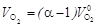 .
.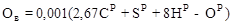 ,
,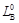 , необходимое для сгорания 1 кг топлива (принимая содержание в воздухе 23% кислорода по массе), кг/кг
, необходимое для сгорания 1 кг топлива (принимая содержание в воздухе 23% кислорода по массе), кг/кг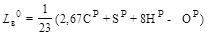 .
.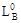 /1,293, т.е. м3/кг
/1,293, т.е. м3/кг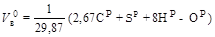
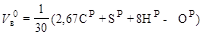 .
.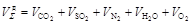 ,
,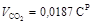 .
.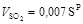 .
.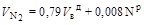 .
.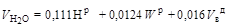 .
.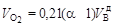 .
.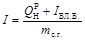
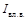 – энтальпия влажного воздуха, определенная по формуле, кДж/кг
– энтальпия влажного воздуха, определенная по формуле, кДж/кг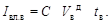 .
. ,
,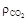 ,
, 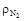 ,
, 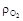 – плотности двуокиси углерода, азота и кислорода соответственно, кг/м3.
– плотности двуокиси углерода, азота и кислорода соответственно, кг/м3. ,
, ,
, 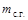 - массы водяных паров и сухих газов соответственно.
- массы водяных паров и сухих газов соответственно.