Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Где/. — избыточное давление над раствором; я — осмотическое давление, которое определяется по формуле (9. 13).Содержание книги
Поиск на нашем сайте
Рис. 12.7. Схема осмоса (а), обратного осмоса (б), диализа и ультрафильтрации (в): 1 — дисперсионная среда (чистая жидкость); 2 — коллоидный или истинный раствор; 3 — мембрана (полупроницаемая перегородка); 4 — поток чистой жидкости (растворителя); 5 — поток примесей Из равенства (12.13) следует, что р>п. (12.14) Условие (12.14) определяет избыточное давление, необходимое для осуществления обратного осмоса. Значение этого давления зависит от осмотического давления, которое для некоторых растворов приведено в параграфе 9.4. Обратный осмос можно использовать, например, для опреснения морской воды. Осмотическое давление морской воды, содержащей 3,5% растворенных солей, составляет 25-105 Па, или примерно 25 атм. Для осуществления обратного осмоса в процессе опреснения морской воды внешнее давление Р должно превышать 25 атм. Морская вода помещается в сосуд 2, в котором в дальнейшем концентрируются примеси (см. рис. 12.7, б), задерживаемые мембраной. Чистая вода проходит через мембрану и собирается в полости 1. Возможности мембранных процессов не исчерпываются обратным осмосом. Так, при помощи диализа, схема которого приведена на рис. 12.7, в происходит очистка дисперсной системы (коллоидного раствора) или раствора ВМС от содержащихся в них примесей в виде ионов или молекул. Очистка обеспечивает устойчивость дисперсных систем. Коллоидный раствор или раствор ВМС помещают в правую часть 2 сосуда, отделенную от левой части 1 мембраной 3. Мембрана проницаема для молекул и ионов, но задерживает частицы дисперсной фазы и макромолекулы ВМС. Примеси в результате диффузии из области большей концентрации (правая часть сосуда) самопроизвольно будут переходить в область меньшей концентрации (левая часть сосуда); поток примесей на рис. 12.7, в показан стрелками 5. Если периодически менять внешний раствор 7, то процесс диффузии и очистки можно ускорить. В результате в области 1 будут соби- раться примеси, которые ранее находились в области 2, а коллоидный раствор или раствор ВМС очистится от них. Интенсифицировать очистку коллоидного раствора при помощи диализа можно путем приложения внешнего давления р (см. рис. 12.7, в). В этом случае процесс называют ультрафиль- траицией: Некоторые важные функции почек человека (выделение отработанных продуктов из крови, регулирование кровяного давления, а также водного и электролитного баланса) достаточно полно воспроизводит искусственная почка, которая работает по принципу диализа и ультрафильтрации. В искусственной почке вследствие диализа и ультрафильтрации происходит удаление из плазмы крови ядовитых продуктов (мочевины, мочевой кислоты, токсинов и др.). Обратный осмос, диализ и ультрафильтрация хотя и применяются для различных целей (см. рис. 12.7), но имеют много общего: используются аналогичная аппаратура и внешнее давление (за исключением диализа). Особенности этих процессов заключаются в механизме и в размере пор. Обратный осмос (см. рис. 12.7, б) в отличие от диализа и ультрафильтрации служит для концентрирования истинных и коллоидных растворов и извлечения растворителя. При обратном осмосе из раствора через полупроницаемую перегородку движется чистый растворитель. По этой причине размер пор мембран должен быть небольшим, менее 1 нм, чтобы через них могли проходить молекулы растворителя и задерживаться молекулы примесей. При диализе и ультрафильтрации (см. рис. 12.7, в) очистки от примесей подвергается коллоидный раствор (высокодисперсные системы типа Т/Ж и Ж/Ж) или раствор ВМС. Через полупроницаемую перегородку движутся примеси, которые находятся в растворенном виде. Размеры частиц дисперсной фазы коллоидных растворов и макромолекул относительно большие. По этой причине поры мембраны должны пропускать примеси и задерживать коллоидные частицы и макромолекулы ВМС. В связи с этим для осуществления диализа и ультрафильтрации размер пор должен быть в пределах от 1 до 10 нм, т.е. большим, чек в случае обратного осмоса. Таким образом, основной принцип действия мембран заключается в избирательной проницаемости, которая определяется размерами пор мембран, свойствами очищаемых систем и внешним давлением. Эффективность мембранных процессов разделения оценивается следующими показателями:
— селективностью где с и с2 — концентрация компонентов исходной смеси и прошедших мембрану:
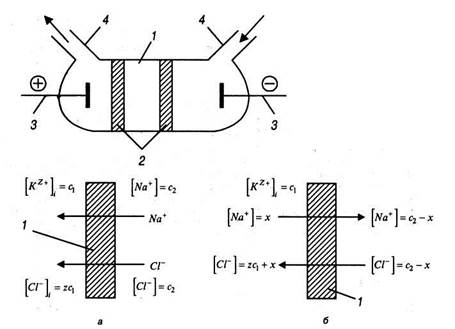
Рис. 12.9. Схема мембранного равновесия Доннана: а — начальное положение; б — после установления равновесия: 7 — мембрана, полупроницаемая перегородка
— коэффициентом разделения к где cAl, cBj и Сд2, Съ2 — концентрация компонентов А и В в исходной смеси и прошедших через мембрану; — Проницаемостью, или удельной производительностью Пу=У/Вт, (12.14, в) где V — объем смеси, прошедшей через мембрану за время т.; В — площадь поверхности мембраны. В процессе обычной фильтрации продукт в виде осадка закрепляется на поверхности фильтра, что приводит к необходимости его периодической регенерации. При использовании мембран раствор и примеси проходят через поровое пространство, а возможность создания избыточного давления в случае обратного осмоса и особенно при ультрафильтрации позволяет избежать или, во всяком случае, резко сократить накопление примесей на поверхности мембран и тем самым исключить необходимость их частой очистки. Для интенсификации процесса очистки с помощью мембран применяют электродиализ, схема которого дана на рис. 12.8. Коллоидный раствор или раствор ВМС / помещают между двумя полупроницаемыми перегородками 2, пропускающими ионы дисперсионной среды. В корпус вмонтированы электроды 3. Совместным воздействием электрического поля и внешнего давления обеспечивают более полное удаление примесей из жидкой дисперсионной среды. Кроме очистки растворов, мембраны способствуют равновесию электролитов в присутствии частиц или ионов, размеры которых не позволяют им проникать через поры этих перегородок; возникает так называемое мембранное равновесие. Схема мембранного равновесия показана на рис. 12.9..По обе стороны полупроницаемой перегородки 1 могут находиться два раствора с концентрациями сх и с2 причем с2> cv Перегородка способна пропускать ионы Na+ и СГ и непроницаема для катионов Kz+, размеры которых соответствуют высокодисперсным системам. Концентрация ионов Na+ и СГ в растворе, находящемся справа от перегородки, больше, чем в растворе слева. Поэтому часть ионов Na+ и С\~ (см. рис. 12.9, а) пройдет через мембрану из области большей концентрации в область меньшей концентрации, т.е. справа налево. В условиях равновесия (см. рис. 12.9, б) концентрация ионов Na+ и СГ справа от мембраны уменьшится на х, слева от мембраны концентрация ионов Кх+ останется неизменной, а концентрация ионов СГ возрастет на х, и появятся ионы Na+ с концентрацией х. Изменение концентрации ионов Na+ и СГ, на величину х и можно определить из условий, когда произведение концентраций диффундирующих ионов в обоих растворах одинаково, т.е. (zcl+x)x=(c2-x)2, (12.15) откуда определится величина х: (12.16) Доля электролита NaCl x/c2 составляет (12.17) Для анализа уравнений (12.16) и (12.17) следует рассмотреть два крайних случая. Первый из них, когда концентрация электролита значительно превышает концентрацию коллоидного раствора, т.е. с2» с, и величиной с, можно пренебречь. В этих условиях из уравнения (12.17) следует х/с2 =1/2 (12.18)
|
||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 229; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.147 (0.009 с.) |