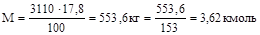Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Особливості реальних хімічних реакцій і виробничих процесівСодержание книги
Поиск на нашем сайте У багатьох випадках рівняння хімічних реакцій лише принципово виражають перебіг процесів. Вони не перебігають до кінця, і для розрахунків за допомогою рівнянь необхідно введення додаткових кількісних характеристик. Причинами неповного перебігу можуть бути: - встановлення в системі хімічної рівноваги; - перебіг побічних процесів за участю одного з реагентів; - припинення процесів до досягнення повного перетворення, наприклад, внаслідок повільного перебігу на кінцевої дільниці. Для характеристики перебігу хімічних реакцій при їх неповному перебігу на практиці використовують наступні показники: - ступінь перетворення (конверсія) вхідних речовин; - вихід продукту. Ступінь перетворення (конверсії) є безрозмірною величиною, що характеризує частку вхідних речовин, що увійшли у реакцію. Якщо співвідношення кількостей реагентів відрізняється від стехіометричного, ступінь перетворення розраховується по речовині, кількість якої є найменшою за стехіометрією. Ступінь перетворення розраховують по формулі:
де М0 – початкова кількість реагенту, по якому розраховують ступінь перетворення; М – поточна кількість реагенту у масі під час відбору проби. Приклад 4.1. В реакцію:
CH3OH + C2H5COOH = C2H5COOCH3 + H2O (2.2)
уведено: - метанолу (CH3OH, М = 32 г/моль) – 5 г; - пропіонової кислоти (C2H5COOH, М = 74 г/моль) – 6 г. Після проведення реакції залишилось 2,66 г метанолу і 0,6 г пропіонової кислоти. Визначити, за якою речовиною слід розраховувати ступінь конверсії ї розрахувати її. Розв’язання: а) розрахуємо кількість молів реагентів, що уведені до реакції: - метанол: - пропіонова кислота: б) співвідношення реагентів, що вступають до реакції у відповідності до рівняння (1.42) складає 1:1. У реакцію введено співвідношення 0,156:0,081 = 1,98:1, що відрізняється від стехіометричного. Метанол знаходиться у надлишку, тому ступінь конверсії слід розраховувати по пропіонової кислоті, якої не вистачає до стехіометричної кількості; в) ступінь перетворення (конверсії) у відповідності з формулою (2.1), складає:
Вихід є безрозмірною величиною, що характеризує частку продуктів реакції, що створилися у порівнянні з тим, що випливає з рівняння хімічної реакції. Він розраховується по формулі:
где М – кількість продукту, що одержано у процесі на практиці (г, кг, моль); Мтеор. – теоретична кількість продукту, що може бути отримана, виходячи з рівняння реакції. Величина Мтеор. може бути розрахована двома способами: ü в розрахунку на повну кількість вхідних речовин, що уводяться в реакцію; ü в розрахунку на кількість вхідних речовин з врахуванням конверсії. В останньому випадку вказують, що вихід розрахований у розрахунку на речовини, що прореагували. Приклад 4.2. Взаємодія хлору з бензолом перебігає у відповідності з рівняннями:
С6Н6 + Cl2 = C6H5Cl + HCl, (2.4)
С6Н6 + 2 Cl2 = C6H5Cl2 + 2HCl. (2.5)
У реакцію уведено суміш з мольним співвідношенням бензол (С6Н6): хлор = 1: 1. Після повного витрачення хлору одержана суміш речовин, що містить: - бензол: 10 % мольн.; - хлорбензол (C6H5Cl): 80 % мольн. - діхлорбензоли (C6H5Cl2): 10 % мольн. Визначити ступінь конверсії бензолу і вихід по хлорбензолу і діхлорбензолам. Втратами речовин у процесі взаємодії зневажити. Розв’язання: а) розрахуємо склад суміші продуктів. Якщо обрати 1 моль суміші, то вона буде містити, у відповідності зі складом,: - бензолу: 0,1 моль; - хлорбензолу: 0,8 моль; - діхлорбензолів: 0,1 моль. б) оскільки усі ці продукти отримані з бензолу, то кількість бензолу, що уведена у реакцію, буде дорівнювати сумарній кількості молів продуктів, що призведені з бензолу, тобто, 1 моль. Звідси, за визначенням, конверсія бензолу складає:
в) обчислимо виходи у розрахунку на повну кількість бензолу. У цьому випадку теоретична кількість хлорбензолу і діхлорбензолів, у відповідності до рівнянь (1.44) і (1.45) складе 1 моль з 1 моль бензолу. Звідси виходи складуть: - по хлорбензолу: 0,8/1 = 0,8 = 80 %; - по діхлорбензолам: 0,1/1 = 0,1 = 10 %; г) обчислимо виходи у розрахунку на бензол, що увійшов у реакцію. Конверсія бензолу 90%, тобто, кількість бензолу, що увійшла у реакції, складає 0,9 моль. Звідси виходи: - по хлорбензолу: 0,8/0,9 = 0,889 = 88,9%; - по діхлорбензолам: 0,1/0,1 = 0,111 = 11,1 % Якщо в хімічної реакції не відбувається змін об’єму – за основу для розрахунків конверсії можна обирати концентрації вхідних речовин (в кг/м3 або кмоль/м3). Якщо в реакції не відбувається виділення газоподібних продуктів, вихід можна розраховувати по масової концентрації в %. Виділення газоподібних продуктів у цьому випадку зменшує загальну масу і дає завищені результати. На практиці для фіксації мас реагентів, складу кінцевої маси і розрахунків виходів і конверсії складається таблиця завантажень. Така таблиця складається для кожного лабораторного експерименту і фіксується в лабораторному журналі. У виробництві такі таблиці входять до складу операційних листків, де фіксуються всі особливості проведення технологічного процесу (його ведуть апаратники) і у операційному журналі, який веде майстер або технолог цеху. Структура таблиці завантажень наведена у табл. 4.1
Таблиця 2.1 – Структура таблиці завантажень
Зміст граф: а) в графу 1 поміщають: - назву кожного продукту, що завантажується (технічного продукту), - назви кожного з компонентів (у тому числі – домішок), що входять до його складу б) в графу 2 поміщають молярні маси (г/моль) кожного з компонентів кожного з продуктів, що завантажується (крім домішок); в) в графу 3 поміщають масові долі кожного з компонентів у складі кожного технічного продукту; г) в графу 4 поміщають масу кожного технічного продукту д) в графу 5 поміщають масу кожного компонента кожного технічного продукту(100 % речовини, що реагує); е) в графу 6 поміщають кількість молів кожного компонента кожного технічного продукту (крім домішок); д) в графу 7 поміщають густину кожного рідкого технічного продукту (її визначають експериментально, або розраховують, спираючись на довідникові дані); е) в графу 8 поміщають об’єм кожного рідкого технічного продукту. На базі такої таблиці становляться прозорими кількості усіх компонентів та співвідношення між ними і легко розраховуються вихід і конверсія, виходячи з експериментальних даних по результатам операцій. Приклад 2.3 В реактор синтезу 2-нітроанізолу було завантажено: - метанолу (вміст основної речовини: 99%, води: 1 %) - 2000 кг; - їдкого натру (NaOH) – 480 кг 53 % водного розчину; - 2-нітрохлорбензолу (2-НХБ, С6H4ClNO2, М = 157,5 г/моль, вміст основної речовини 99%, домішок 1 %) – 630 кг. При нагріві перебігає реакція:
C6H4ClNO2 + NaOH + CH3OH = C6H4(NO2)(OCH3) + NaCl + H2O. (2.6)
Після завершення процесу вміст 2-нітроанізолу (C6H4(NO2)(OCH3), М = 153 г/моль) у кінцевої масі склав 17,8 %. Скласти таблицю завантажень і визначити вихід з 2-нітроанізолу. Розв’язання: а) оскільки серед продуктів реакції немає газоподібних речовин, то маса продуктів, що одержані наприкінці процесу, дорівнює початковій масі:
М0 = 2000+480+630 = 3110 кг;
б) розраховуємо масу 100%-го 2-нітрохлорбензолу, оскільки він самий буде реагувати:
M2-НХБ = 630×0,99 = 623,7 кг;
в) розраховуємо масу 100%-го NaOH: M=480×53/100 = 254,4 кг; по залишку – розраховуємо кількість води г) розраховуємо кількість молів і об’єми кожної з рідких речовин Результати розрахунків вносимо у таблицю завантажень (табл. 1.6). З неї випливає, що найменша кількість у порівнянні зі стехіометрією спостерігається у 2-НХБ; д) розраховуємо кількість 2-нітроанізолу в масі в кг і молях:
вихід 2-нітроанізолу по 2-НХБ:
Таблиця 2.2– Таблиця завантажень на операцію синтезу
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 167; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.151 (0.007 с.) |

 , (2.1)
, (2.1) моль;
моль;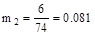 моль;
моль;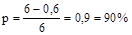
 , (2.3)
, (2.3)