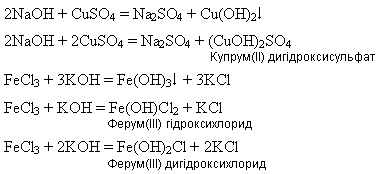Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Хімічні властивості гідроксидів лужних металів.Содержание книги
Поиск на нашем сайте
Гідроксиди натрію та калію роз’їдають тканини, шкіру, органічні речовини, тому їх називають їдкими лугами. дисоціація на йони: 1.Дисоціація У водних розчинах гідроксиди лужних металів повністю дисоціюють на йони:
2.дія на індикатори: *пригадайте,як діють луги на індикатори 3.взаємодія з кислотами: Гідроксиди лужних металів вступають у реакцію нейтралізації з кислотами, утворюючи середні або кислі солі та воду: 2NaOH + H2SO4 = Na2SO4 + 2H2O NaOH + H2SO4 = NaHSO4 + H2O *напишіть як будуть взаємодіяти луги з фосфатною,карбонатною,хлоридною та нітратною кислотою.Які солі будуть утворюватись при надлишку одного з реагентів? 4.взаємодія з кислотними оксидами: 2KOH + SO3 = K2SO4 + H2O 2NaOH + SiO2 = Na2SiO3 + H2O - сплавляння *напишіть рівняння реакцій взаємодії лугів з вуглекислим газом,сульфур (4)оксидом,оксидом фосфору(5). 5.взаємодія з амфотерним оксидами: 2NaOH + ZnO = Na2ZnO2 + H2O – сплавляння 2KOH + Al2O3 = 2KAlO2 + H2O - сплавляння 6.взаємодія з амфотерним гідроксидами: 2NaOH + Zn(OH)2 = Na2ZnO2 + 2H2O – сплавляння 2NaOH + Zn(OH)2 = Na2[Zn(OH)4] - у розчині 7.взаємодія з металами, яким відповідають амфотерні гідроксиди:
8.взаємодія з солями Реакція між гідроксидами і солями відбувається за типом реакції обміну, яка проходить тільки в розчині, при цьому утворюються або основні солі, або нерозчинні у воді основи:
*допишіть рівняння реакцій,складіть повне та скорочене іонне рівняння FeCl3 + 3 NaOH = Cr(NO3)2 + 2 KOH = 9.взаємодія з натрій ацетатом:
10.взаємодія з галогенами:
11.взаємодія з жирами: Під дією лугів на рослинні олії або тваринніжири утворюються розчинні солі вищих карбонових кислот, які є основною складовою частиною мила:
Добування лугів. *на основі знань про основні класи неорганічних сполук запропонуйте кілька способів добування лугів 1) 2) 3) Застосування лугів. Луги застосовують у виробництві фарб, мила, штучного волокна, паперу, текстилю, очищення нафтопродуктів та ін. * Na→Na2O→NaOH→Na2SO4→Na→Na2S *K→KOH→KCI→K2SO4→ KOH→K3AIO3 *Добудьте,використовуючи калій, кисень,воду,сульфатну кислоту,як найбільше сполук Лужно-земельні метали *напишіть електронну конфігурацію атомів кальцію,барію,магнію.Спрогнозуйте їх властивості. До ІІ групи, головної підгрупи періодичної системи, входять Берилій Ве, Магній Mg, Кальцій Ca, Стронцій S r, Барій Ba, Радій Ra. Елементи Ca, Sr, Ba, Ra і відповідні прості речовини мають групову назву – лужноземельні метали, оскільки їх гідроксиди є лугами, а їх тугоплавкі оксиди раніше називали землями. Кальцій Кальцій Са входить до складу гірських порід і мінералів, міститься в грунті, живих організмах і природних водах. З кальцій карбонату побудовані корали, черепашки молюсків тощо.
|
|||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 443; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.126 (0.007 с.) |