Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Какими путями при обмене амк обр-ется аммиак, роль глутамина и аспарагина в обмене в-в.Содержание книги
Поиск на нашем сайте Дезаминирование АМК Доказано существование 4 типов дезаминирования АМК (отщепление аминогруппы). Во всех случаях NH2-группа АМКы освобождается в виде аммиака.
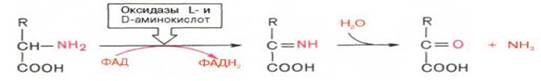
Помимо аммиака, продуктами дезаминир явл ЖКы, оксик-ты и кеток-ты. Для жив тканей, раст и больш-ва аэробных микроорг-мов преобладающим типом р-ций явл окислительное дезаминирование АМК, за исключением гис-тидина, подвергающегося внутримол-лярному дезаминированию. Рассм более подробно мех-м окислительного дезаминиро-вания АМК, протекающего в две стадии.
1-ая стадия явл ф-тативной и завершается обр-нием неустойчивого промежут продукта (иминок-та), к-рый на 2-ой стадии спонтанно без участия ф-та, но в присутствии воды распад-ся на аммиак и α-кеток-ту. Следует указать, что оксидазы АМК (L- и D-изомеров) явл-ся сложными флавопротеинами, содер в кач-ве коф-та ФМН или ФАД, к-рые выполняют в этой р-ции роль акцепторов 2 электронов и протонов, отщепл-ся от АМКы. Оксидазы L-АМК могут содержать как ФМН, так и ФАД, а оксидазы D-АМК – только ФАД в качестве простетической группы. Схематически р-ции окислительного дезами-нирования АМК с участием коф-тов могут быть представлены в следующем виде:
Восст-ные флавиннуклеотиды оксидаз L- и D-АМК могут непосредств окисляться мол-лярным кислородом. При этом обр-ется перекись водорода, к-рая подверг-ся расщеплению под действием каталазы на воду и кислород. В животных тканях оксидазным путем со значительно большей скоростью дезами-нируются D-изомеры АМК. Эти данные подтвердились после того, как из животных тканей был выделен специфический ф-т оксидаза D-АМК, к-рый в отличие от оксидазы L-АМК оказался высокоактивным при физиологич знач рН среды. Не до конца ясным остается вопрос о том, каково значение столь активной оксидазы D-АМК в тканях, если поступающие с пищей белки и белки тела животных и человека состоят исключительно из природных (L-изомеров) АМК. В жив тканях открыт высокоакт-ый при физиологич знач рН специфич ф-т (глутаматдегидрогеназа), катал-щий окислит дезаминирование L-глутаминовой к-ты. Он явл анаэробным ф-том и чрезвычайно широко распростр во всех живых объектах. В качестве коф-та глутамат-дегидрогеназа содержит НАД (или НАДФ). Р-ция включает анаэробную фазу дегидрирования глутаминовой к-ты с обр-нием промежуточного продукта – иминоглутаровой к-ты и спонтанный гидролиз последней на аммиак и α-кетоглутаровую к-ту в соотв-ии со следующей схемой:
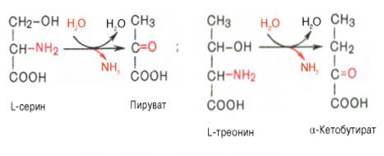
1-я ст окисл глутаминовой к-ты аналогична р-ции окисл-ного дезаминирования. Восст-нный НАДН окисляется при участии флавиновых ф-тов и цитохромной с-мы с обр-нием конечного продукта воды. Обр-шийся аммиак благодаря обратимости ф-тативной р-ции, но обязательно в присутствии восст-ного НАДФН может уч-ть в синтезе глутамата из α-кетоглутаровой к-ты. Различают 3 разных типа глутаматдегидрогеназ: 1 из них исп-ет в кач-ве коф-та как НАД, так и НАДФ (кл жив-ых); 2 др исп или НАД, или НАДФ (микроорг-мы, кл раст и грибов), соотв-но катал-руя дезаминир или биосинтез глутамата. Глутаматдегидрогеназа животных тканей явл одним из наиболее изученных ф-тов азотистого обмена. Это олигомерный ф-т (мол. масса 312000), состоящий из 6 субъединиц (мол. масса каждой около 52000) и проявляющий свою основную активность только в мультимерной форме. При диссоциации этой мол-лы на субъединицы, наступающей легко в присутствии НАДН, ГТФ и нек-рых стероидных гормонов, ф-т теряет свою главную глутаматдегидрогеназную ф-цию, но приобретает способность дезаминировать ряд других АМК. Это свидетельствует об аллостерической природе глутаматдегидрогеназы, действующей как регуляторный ф-т в АМКном обмене. Помимо перечисленных 4 типов дезаминирования АМК и ф-тов, кат-ющих эти превращения, в животных тканях и печени человека открыты также три специфических ф-та (серин- и треонин-дегидратазы и цистатионин-γ-лиаза), кат-ющих неокислительное дезаминирование соотв-енно серина, треонина и цистеина.
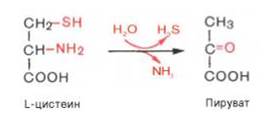
Конечными продуктами р-ции явл пируват и α-кетобутират, аммиак и сероводород. Поскольку указанные ф-ты требуют присутствия пиридоксальфосфата в качестве коф-та, р-ция неокислительного дезаминирования, вероятнее всего, протекает с обр-нием шиффовых оснований как промежуточных метаболитов.
Билет №3 1. Витамин D (кальциферол; антирахитический вит) сущ-ет в виде нескольких соед, различ-хся как по хим строению, так и по био активности. Для ч-ка и жив активными препаратами считаются витамины D2и D3. В природных продуктах содержатся преимущественно провитамины D2и D3– соответственно эргостерин и холестерин. С хим т.зр. эргостерин(ол) предст собой одноатомный ненасыщ циклический спирт, в основе стр-ры к-рого лежит конденсированная кольцевая система циклопентанпергидрофенантрена. Под действием УФ-лучей эргостерин через ряд промежуточных продуктов (люмистерин, тахистерин) превращается в витамин D2:
Витамин D2образуется из эргостерина в результате разрыва связи между 9-м и 10-м углеродными атомами кольца В под действием УФ-лучей. Предшественником витамина D3 явл холестерин:
Благодаря наличию холестерина и 7-дегидро-холестерина в сост липидов кожи ч-ка возможен синтез витамина D3при солнечном облучении или облучении лампой УФ излучения поверхности тела. Этим приемом особенно широко пользуются при лечении рахита у детей. Витамины D2и D3 предст собой б/цв кристаллы с темп-рой плав 115–117°С, нерастворимые в воде, но хорошо растворимые в жирах, хлороформе, эфире и других жирорастворителях. Недостаток витамина D в рационе детей приводит к возникновению широко известного заболевания – рахита, в основе развития которого лежат изменения фосфорно-кальциевого обмена и нарушение отложения в костной ткани фосфата кальция. Поэтому основные симптомы рахита обусловлены нарушением нормального процесса остеогенеза. Развивается остеомаляция – размягчение костей. Кости становятся мягкими и под тяжестью тела принимают уродливые О- или Х-образные формы. На костно-хрящевой границе ребер отмечаются своеобразные утолщения – так называемые рахитические четки. У детей, больных рахитом, относительно большая голова и увеличенный живот. Развитие последнего симптома обусловлено гипотонией мышц. Нарушение процесса остеогенеза при рахите сказывается также на развитии зубов; задерживаются появление первых зубов и формирование дентина. Для авитаминоза D взрослых характерной особенностью является развитие остеопороза вследствие вымывания уже отложившихся солей; кости становятся хрупкими, что часто приводит к переломам. Био роль. вит D выполняет свои био ф-ции в организме в форме обр-щихся из него актив метаболитов, в частности 1,25-диоксихолекальциферола и 24,25-диоксихолекальциферола, причем если гидрокси-лирование в 25-м положении осуществляется в печени, то этот процесс в 1-м положении протекает в почках. Ферменты, кат-ющие эти р-ции, наз гидроксилазами, или монооксигеназами. В реакциях гидрокси-лирования используется мол-рный кислород. Показано, что специфическая lα-гидроксилаза содержится, помимо почек, в костной ткани и плаценте. 1,25(OH)2D3участвует в регуляции процессов всасывания Са и Р в кишечнике, резорбции костной ткани и реабсорбции Са и Р в почечных канальцах. Процессы остеогенеза и ремоделирования костной ткани, напротив, регулируются 24,25(OH)2D3. 1,25(OH)2D3в ядрах кл органов (почки, мозг, поджелудочная железа, гипофиз, мол железа), где он способствует синтезу мРНК, Са-связывающих белков и гормонов, регулирующих обмен кальция; в то же время он не обнаруживается в печени, селезенке, скелетной и сердечной мышцах. Распространение в природе и суточная потребность. Наибольшее количество витамина D3содержится в продуктах животного происхождения: сливочном масле, желтке яиц, печени и в жирах, а также в рыбьем жире, который широко используется для профилактики и лечения рахита. Из растительных продуктов наиболее богаты витамином D2растительные масла (подсолнечное, оливковое и др.); много витамина D2в дрожжах. Случаи гипервитаминоза D у людей наблюдаются при «ударной» терапии рахита и некоторых дерматозов (волчанка). Гипервитаминоз был отмечен после приема более 1500000 ME витамина D в сутки. Прием очень больших доз витамина D может вызвать смертельный исход. У экспериментальных животных гипервитаминоз сопровождается увелич отложения гидроксилапатита в костях и некоторых внутренних органах. У собак, например, отмечена кальцификация почек. Все эти симптомы исчезают после прекращения приема витамина
|
||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 380; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.151 (0.007 с.) |