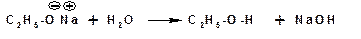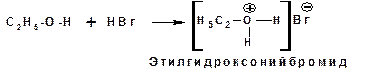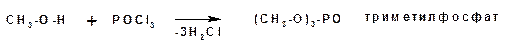Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Реакции с разрывом связи О-Н
Кислотно-основные свойства Спирты являются амфотерными соединениями. Они способны выступать в роли как кислот, так и оснований. Диссоциацией по связи О-Н, спирты проявляют себя как типичные кислоты Бренстеда:
Соответственно спирты способны взаимодействовать со щелочными и щелочноземельными металлами (магний) с замещением атома водорода гидроксильной группы на катион металла. При этом выделяется водород (в момент выделения «in sity» атомарный и поэтому очень активный) и образуется алкоголят:
Алкоголяты легко гидролизуются:
Кислотные свойства спиртов понижаются в ряду метиловый, первичный, вторичный, третичный, что обусловлено электронодонорными свойствами алкильных групп, понижающих стабильность аниона. Свойства оснований спирты проявляют по отношению как к кислотам Бренстеда, так и к кислотам Льюиса. Донорным атомом в молекуле спирта является атом кислорода. Кислоты Бренстеда протонируют атом кислорода гидроксильной группы:
Кислоты Льюиса образуют со спиртами донорно-акцепторные комплексы, в которых атом кислорода выступает в роли донора неподеленной электронной пары:
Спирты являются слабыми основаниями. Основные свойства возрастают в ряду: метиловый, первичный, вторичный, третичный, что обусловлено электронодонорными свойствами алкильных групп.
Этерификация Спирты взаимодействуют с минеральными и органическими кислотами с образованием соответствующих сложных эфиров и воды:
Эфиры неорганических кислот получаются при взаимодействии спиртов и хлорангидридов неорганических кислот:
Образование уксусноэтилового эфира:
Дегидратация При действии на спирты водоотнимающих веществ происходит межмолекулярное и внутримолекулярное отщепление воды. Водоотнимающими веществами являются кислоты: серная, фосфорная, щавелевая, беннзолсульфокислота; оксиды металлов: оксид алюминия, оксид тория. При межмолекулярной дегидратации образуются простые эфиры. Механизм реакции включает две стадии. На первой стадии образуется сложный эфир, который на второй стадии вступает в реакцию нуклеофильного замещения со второй молекулой спирта:
В случае внутримолекулярной дегидратации спиртов, протекающей при более высокой температуре, от сложного эфира минеральнлй кислоты отщепляется кислота с образованием непредельного соединения. В этом случае на второй стадии протекает реакция элиминирования:
При этом водород отщепляется в соответствии с правилом Зайцева, с образованием наиболее алкилированного олефина. Эта закономерность в сочетании с правилом Марковникова дает возможность переходить от одних спиртов к другим. Например, от изобутилового к третичному бутиловому спирту:
1.4.1.4. Реакции с галогеналканами. Спирты являются слабыми нуклеофилами поэтому практически не реагируют с галогеналканами. Исключение составляют аллил и бензилгалогениды и некоторые третичные галогенпроизводные. Реакции протекают по механизму SN1. Алкоксид-анионы являются сильными нуклеофилами и основаниями и способны реагировать с галоидными алкилами по механизму SN2:
|
|||||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 161; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.245.245 (0.007 с.) |