Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Построение калибровочной кривой
Для построения калибровочной кривой используют чистые препараты белка, например, кристаллические препараты гемоглобина, бычьего сывороточного альбумина и другие. Для приготовления исходного раствора белка отвесить 0,1 г стандартного белка и растворить в 100 мл дистиллированной воды. Раствор отфильтровать. Точную концентрацию приготовленного раствора устанавливают по методу Кьельдаля. Для этого берут на сжигание в колбы Кьельдаля 3 пробы исходного раствора белка по 5 мл. приливают в колбу 7 мл концентрированной Н2SО4 d=1,84. Равномерное озоление пробы начинается уже при комнатной температуре, залитые навески оставляют на ночь. На следующий день колбы ставят на электроплитку и проводят постепенное сжигание в начале при слабом нагреве, затем при сильном, осторожно взбалтывая. Сжигание проводят в присутствии катализатора (2-3 мл перекиси водорода), до полного обесцвечивания раствора. Содержимое колбы Кьельдаля количественно переносят горячей дистиллированной водой в мерную колбу на 500 мл, охлаждают, перемешивают и доводят раствор в колбе до метки. Содержание в растворе аммония устанавливают по калибровочной кривой образцовых растворов. Для ее построения одновременно с испытуемым раствором готовят образцовые растворы. В мерные колбы на 100 мл помещают 0,2; 0,5; 1; 2; 4 мл рабочего образцового раствора NH4Cl, затем 4 мл раствора сегнетовой соли, добавляют воды до половины объема, 4 мл реактива Несслера и доводят объем дистиллированной водой до метки. Образцовый раствор NH4Cl готовят растворением 0,7405 г химически чистого перекристаллизованного аммония хлористого в дистиллированной безаммиачной воде и доводят объем до 1 л, 20 мл этого раствора переносят в мерную колбу на 1 л, доводят объем до метки; 1 мл этого раствора содержит 0,005 мг NH4+, его используют для приготовления образцовых растворов. Просмотр окраски производят через 10 минут после прибавления реактива Несслера на приборе фотоколориметре: КФК-3 при длине волны λ=400 нм. Содержание аммонийного азота рассчитывают по формуле:
Н – навеска, г; С – объем раствора, взятый для окрашивания, мл (10). При пересчете содержания азота на белок используют универсальный белковый коэффициент – 6,25.
Из исходного раствора методом разведения приготовить растворы с меньшим содержанием белка по приведенной схеме. Для этого условно принимают концентрацию исходного раствора белка за 100 единиц. 1. Исходный раствор – 100 ед. белка 2. 8 мл р-ра 1 + 2 мл Н2О – 80 ед. белка 3. 7 мл р-ра 1 + 3 мл Н2О – 70 ед. белка 4. 6 мл р-ра 1 + 4 мл Н2О – 60 ед. белка 5. 5 мл р-ра 1 + 5 мл Н2О – 50 ед. белка 6. 5 мл р-ра 2 + 5 мл Н2О – 40 ед. белка 7. 5 мл р-ра 3 + 5 мл Н2О – 35 ед. белка 8. 5 мл р-ра 4 + 5 мл Н2О – 30 ед. белка 9. 5 мл р-ра 5 + 5 мл Н2О – 25 ед. белка 10. 5 мл р-ра 6 + 5 мл Н2О – 20 ед. белка 11. 5 мл р-ра 8 + 5 мл Н2О – 15 ед. белка 12. 5 мл р-ра 10 + 5 мл Н2О – 10 ед. белка 13. 5 мл р-ра 11 + 6 мл Н2О – 5 ед. белка Во всех приготовленных растворах провести определение белка по методу Лоури. В качестве контроля использовать пробу, в которой вместо раствора белка была взята дистиллированная вода. Результаты занести в таблицу 14. Таблица 14.
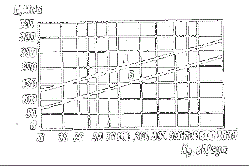
По полученным данным на миллиметровой бумаге построить калибровочную кривую в координатах «оптическая плотность – концентрация белка». Калибровочная кривая используется для определения белка при выполнении работы.
Оформление результатов Полученные результаты записать в таблицу 15. Таблица 15.
5.4 Контрольные вопросы 1. Какие белки называют запасными белками семян растений? 2. Назовите характерные особенности белков пшеницы глиадина и глютенина. 3. Какова роль клейковины в определении хлебопекарных достоинств пшеницы? 4. Назовите аминокислотный состав белков клейковины. 5. Назовите характерные особенности и показатели качества клейковины. 6. Что такое глютатион? 7. Перечислите функции глютатиона в обмене веществ. Литература [1, c.112-124]
|
|||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 403; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.26.152 (0.005 с.) |
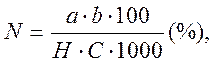 где
где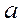 - количество азота по графику, мг;
- количество азота по графику, мг;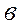 - общий объем раствора, мл (500);
- общий объем раствора, мл (500);