Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кислородсодержащие соединения галогенов
Галогены непосредственно с кислородом не взаимодействуют. Это обусловлено небольшой энергией связи Г–О и невозможностью использовать высокие температуры для осуществления реакций окисления, т.к. для них Cl2 + 2O2 = 2ClO2
S D Н D G Из соединений кислорода с фтором наиболее устойчив фторид кислорода OF2. Хлор образует четыре оксида в степенях окисления +1, +4, +6, +7. Оксиды брома менее устойчивы, существуют лишь при температурах ниже 0ºС. Иод имеет относительно устойчивый оксид в степени окисления йода +5:
Все оксиды хлора – кислотные оксиды. Им соответствуют кислоты:
Кислотные оксиды хлора реагируют с водой, с основными оксидами, основаниями. Оксидам Cl2O, Cl2O7 соответсвуют кислоты HClO, HClO4: H2O + Cl2O = 2HClO; Cl2O7 + H2O = 2HClO4. В темноте СlО2 может сохраняться без изменений в течение длительного срока. При действии света на ClO2 в присутствии воды или в щелочи происходит реакция диспропорционирования: 6ClO2 + 3H2O = HCl + 5HClO3; 2ClO2 + 2NaOH = NaClO2 + NaClO3 + H2O. При действии на ClO2 ультрафиолета или озона образуется другой взрывоопасный оксид хлора Cl2O6. Молекула ClO3 парамагнитна, поэтому в жидком состоянии полностью димеризована. В парах существуют малостабильные молекулы ClO3. В чистом состоянии оксид достаточно устойчив, однако взрывается при соприкосновении с органическими соединениями, бурно реагирует с водой и со щелочами (реакция диспропорционирования):
Cl2O6 + H2O = HClO3 + HClO4; 2ClO3 + 2NaOH = NaClO3 + NaClO4 + H2O. I 2 O 5 – это единственный термодинамически устойчивый оксид из всех оксидов галогенов ( 2НIO3 Разложение кислоты осуществляется при температуре 240°С. Выше 300°С оксид разлагается на простые вещества: 2I2O5 I2O5 быстро растворяется в воде с образованием кислоты. Одно из применений I2O5 – определение содержания оксида углерода (II). Анализ основан на реакции: 5СО + I2O5 = I2 + 5СО2. I2O5 проявляет окислительные свойства, восстанавливаясь до I2, содержание которого определяют титрованием с тиосульфатом натрия. Кислородсодержащие кислоты галогенов, за исключением HClO4, в свободном виде не выделены, существуют только в растворах. Кислородсодержащие кислоты галогенов:
Кислоты неустойчивы, проявляют окислительные свойства. Самым сильным окислителем является HClO, самой устойчивой кислотой является HClO4. Возрастание силы кислот хлора с повышением степени окисления связано с увеличением количества атомов кислорода, которые оттягивают на себя электронную плотность, в результате чего ослабевает прочность связи Н – О:
Пространственная конфигурация соответствующих кислот различна, хотя во всех этих соединениях орбитали хлора находятся в состоянии sp 3-гибридизации. Структура ионов меняется от линейной (С1О–), уголковой (С1O
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 55; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.128.173.155 (0.009 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
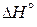 > 0, ∆ S
> 0, ∆ S  < 0:
< 0: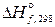 , кДж/моль 0 0 104,6
, кДж/моль 0 0 104,6 , Дж/(моль × К) 223 205,04 251,3
, Дж/(моль × К) 223 205,04 251,3 I2O5 + H2O
I2O5 + H2O
 Сl2О
Сl2О

 СlО2
СlО2
 Сl2О6
Сl2О6

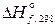 = –184,5 кДж/моль). Его получают при нагревании иодноватой кислоты:
= –184,5 кДж/моль). Его получают при нагревании иодноватой кислоты: I2O5 + Н2О.
I2O5 + Н2О.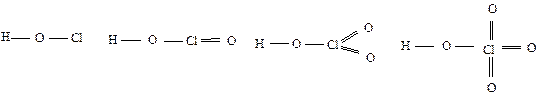
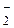 ) до пирамидальной (С1O
) до пирамидальной (С1O  ) и тетраэдрической (С1O
) и тетраэдрической (С1O 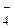 ). При переходе от С1О– к С1O
). При переходе от С1О– к С1O