Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Решение задач с изменением концентрации растворов ⇐ ПредыдущаяСтр 4 из 4
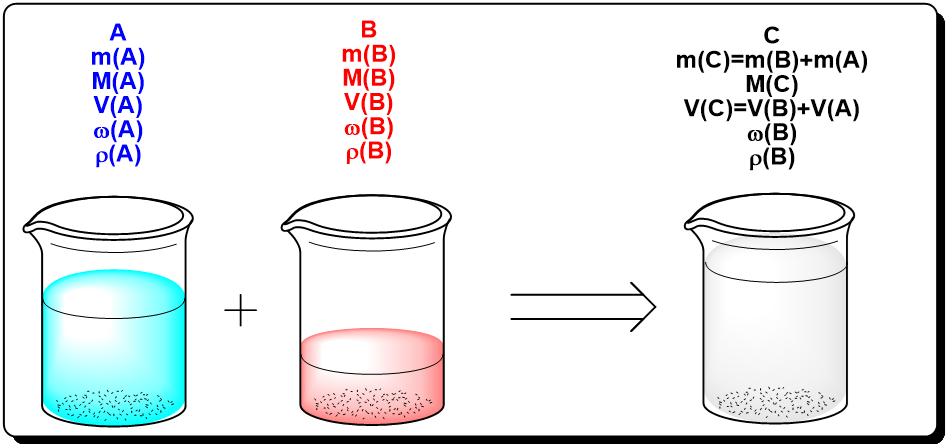
Общие принципы решения задач с изменением концентрации растворов При решении задач с изменением концентрации растворов необходимо помнить, что характеристики (m, V, ω и пр.) даны для разных растворов: исходного и полученного. Важно не перепутать эти характеристики между собой. Поэтому рекомендуется обозначать растворы цифрами 1,2,3 и ставить соотвествующие индексы у величин. Например, масса первого раствора будет записана так: m1(p−pa), а массовая доля вещества во втором растворе: ω2. Если решение таких задач вызывает у вас трудности, то попытайтесь себе представить этот процесс (упаривание, разбавление, смешение и пр.) с помощью схематичного рисунка:
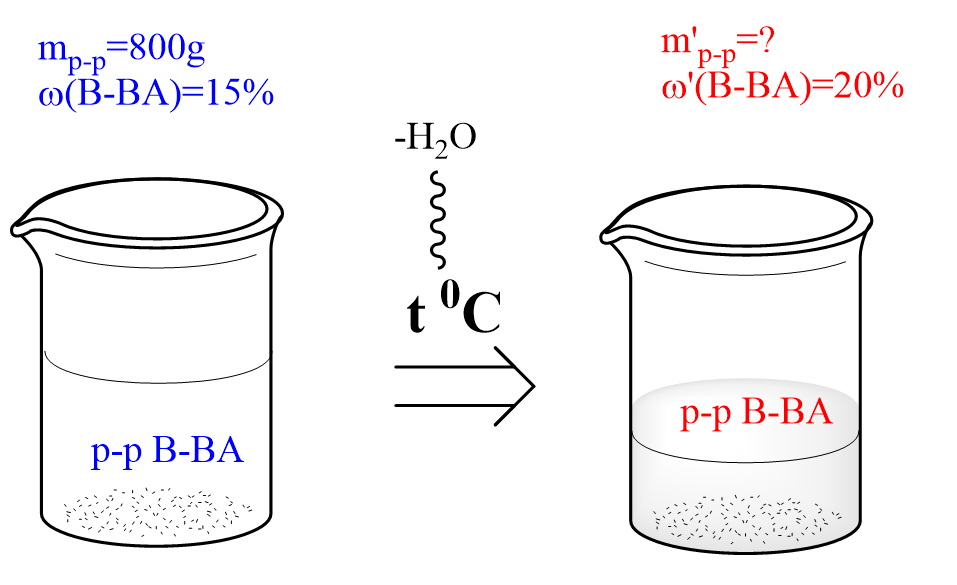
Решение задач на упаривание растворов При решении данного типа задач, следует помнить, что в большинстве случаев испаряется вода, и, следовательно уменьшается масса полученного раствора. Масса вещества, как правило, остается неизменной. В некоторых случаях испаряться может само вещество, это обусловлено химическими свойствами вещества (например, аммиак) и(или) будет прописано в условиях задачи. Задача Сколько граммов воды надо испарить из 800 г 15%-го раствора вещества, чтобы увеличить его массовую долю на 5%? Решение ДАНО: ω(в-ва)=15%=0,15 m(p-pa)=800г ω'(в-ва)=(15+5)%=20%=0,2 НАЙТИ: mисп.(H2O)=? РЕШЕНИЕ: 1)Найдем массу растворенного вещества в исходном растворе: m(в-ва)=ω(в-ва) ⋅ m(p−pa)=0,15 ⋅ 800г=120г 2) Поскольку испаряется только вода, масса вещества остается неизменной: m(в-ва) = m'(в-ва)=120г 3) Зная массу растворенного вещества и его массовую долю, найдем массу полученного раствора: m′(р-ра)=m(в-ва)/ω(в-ва)=120г/0,2=600г Масса испаренной воды - разность масс полученного и исходного растворов: mисп.(H2O)= m(р-ра) - m'(р-ра) = 800г - 600г = 200г ОТВЕТ: нужно испарить 200г воды
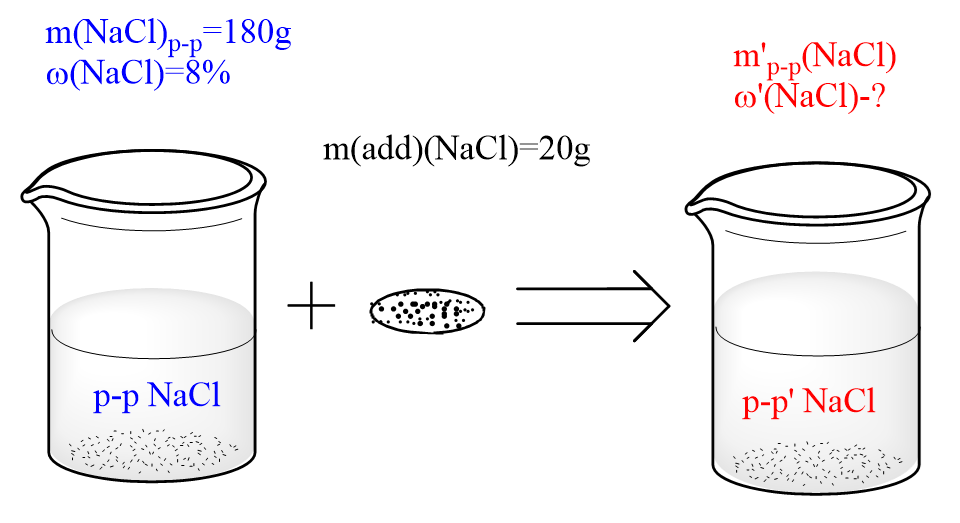
РЕШЕНИЕ ЗАДАЧ НА концентрирование РАСТВОРОВ (добавление вещества) При решении таких задач важно понимать, что при добавлении вещества концентрация раствора увеличивается, то есть масса вещества в полученном растворе = масса вещества в исходном растворе + масса добавленного вещества. Задача К 180 г 8-%-ного раствора хлорида натрия добавили 20 г NaCl. Массовая доля хлорида натрия в образовавшемся растворе равна __ %. Решение
Дано: W (NaCl)=8%=0,08 m(p-pa)=180г mдоб(NaCl) =20г НАЙТИ: ω'(NaCl)=? РЕШЕНИЕ: 1)Найдем массу образовавшегося раствора: m’(p-pa)= m(p-pa) + mдоб (NaCl) = 180г + 20г = 200г 2) Найдем общую массу хлорида натрия в образовавшемся растворе: m’(NaCl) = m(NaCl) + m доб (NaCl) Для этого сначала посчитаем массу m(NaCl) в начальном растворе: m(NaCl)=ω(NaCl) ⋅ m(p−pa)/100%=8% ⋅ 180г/100%=14,4г m’(NaCl)= m(NaCl) + mдоб (NaCl) = 14.4г + 20г=34.4г 3) Найдем массовую долю соли в полученном растворе: ω′(NaCl)=m′(NaCl)/m′(p−pa) ⋅ 100%=34,4г/200г ⋅ 100%=17,2% Ответ: 17,2%
|
|||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 240; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.179.54 (0.006 с.) |