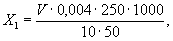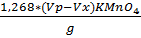Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Массовая концентрация щелочи в пересчете на NaOH ⇐ ПредыдущаяСтр 3 из 3
25 см3 раствора А, переносят пипеткой в коническую колбу и осторожно небольшими порциями прибавляют 10 см3 раствора перекиси водорода, осторожно перемешивая во избежание сильного газовыделения. Через 2-3 мин после прекращения интенсивного газовыделения в колбу прибавляют 2-3 капли фенолфталеина и титруют ее содержимое раствором соляной кислоты до обесцвечивания раствора.
Массовую концентрацию щелочи в пересчете на NaOH(X 1), г/дм3, вычисляют по формуле: где V - объем раствора соляной кислоты концентрации точно 0,1 моль/дм3, израсходованный на титрование, см3; 0,004 - масса гидроксида натрия (г), соответствующая 1 см3 раствора соляной кислоты концентрации точно 0,1 моль/дм3. Хлорное железо FeCl 3 Определение плотности хлорного железа
Ареометр 1,360-1,420 2)Определение содержания хлорного железа FeCl 3 В коническую колбу с притертой пробкой на аналитических весах весах взвешиваем 1,5г. анализируемого продукта. Добавляем 50 мл дистиллированной воды, 10 мл 25% HCl, 15 мл 20% раствора KY. Быстро закрываем колбу пробкой, смоченной 20% раствором KY, перемешиваем и оставляем в темном месте на 10 минут. Затем смываем пробку дистиллированной водой в эту же колбу, доводим объем в колбе до 100 мл и титруем 0,1 н. раствором Na2S2O3 до бледно желтого окрашивания раствора, добавляем 2 мл 1% крахмала и дотитровываем до обесцвечивания раствора. Одновременно проводим холостое определение с тем же количеством реактивов, но без анализируемого продукта.
FeCl3 = 3)Определение содержания хлористого железа FeCl 2 Берём коническую колбу на 250 мл, взвешиваем 2г пробы на аналитических весах, добавляем 75 мл кипяченной дистиллированной воды, 20 мл смеси Рейнгарда-Циммермана. Сначала титруем холостую пробу KMnO4 0,1н, а затем колбу с пробой, сравнивая с холостой.
FeCl2 =
Определение содержания HCl Берём коническую колбу на 250 мл, взвешиваем 1г пробы на технических весах, добавляем 10 мл дистиллированной воды и титруем 1н NaOH до выпадения осадка.
Хлористое железо FeCl 2 Определение содержания HCl Берём коническую колбу на 250 мл, взвешиваем 1г пробы на технических весах, добавляем 10 мл дистиллированной воды, индикатор бромкрезоловый зелёный и титруем 0,1н NaOH до зелёного цвета раствора.
2)Определение содержания FeCl 2 Берём коническую колбу на 250 мл, взвешиваем 0,5г пробы на аналитических весах, добавляем 75 мл кипяченной дистиллированной воды, 20 мл смеси Рейнгарда-Циммермана. Сначала титруем холостую пробу KMnO4 0,1н, а затем колбу с пробой, сравнивая с холостой.
FeCl2 =
Заключение: Во время прохождения практики в производственной лаборатории: 1. Приобрела опыт работы по исследованию проб с использованием новых методик, требующих серьезной теоретической и практической подготовки для проведения анализа. 2. Закрепила приобретенные во время обучения в техникуме теоретические знания, умения и навыки проведения лабораторных работ, расчетов. 3. Приобрела опыт работы в трудовом коллективе. 4. Изучила структуру предприятия. Вывод: В процессе прохождения производственной практики закрепила навыки и умения, полученные за весь период обучения в техникуме, а также, благодаря выполнения работы лаборанта, формировалась система общих и профессиональных компетенций, которые являются oсновополагающими в дальнейшей профессиональной деятельности. Литературный обзор.?
Статистическая обработка
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2019-08-19; просмотров: 758; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.2.213 (0.007 с.) |
||||||||||||||||||||