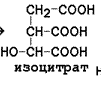Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Перечислите окислительные реакции цикла Кребса, укажите их биологическое значение. Напишите реакцию цикла, катализируемую ФАД-зависимой дегидрогеназой.
1) дегидрирование изоцитрата с последующим выделением молекулы СО2 (декарбоксилированием) и образованием α-кетоглутарата (рис. 12.6, реакция 4). Это – первая окислительно-восстановительная реакция в цикле Кребса, в результате которой образуется НАДН. Изоцитратдегидрогеназа, катализирующая реакцию, - регуляторный фермент, активируется АДФ. Избыток НАДН ингибирует фермент. 2) окислительное декарбоксилирование α-кетоглутарата, катализируется мультиферментным комплексом (рис. 12.7, реакция 5), сопровождается выделением СО2 и образованием второй молекулы НАДН. Эта реакция аналогична пируватдегидрогеназной реакции. Ингибитором служит продукт реакции – сукцинил-КоА. 3) дегидрирование сукцината с образованием фумарата и молекулы ФАДН2 (рис. 12.7, реакция 7). Фермент сукцинатдегидрогеназа прочно связан с внутренней мембраной митохондрии.
4) дегидрирование малата, приводящее к образованию оксалоацетата и третьей молекулы НАДН (рис.12.7, реакция 9). Образующийся в реакции оксалоацетат может вновь использоваться в реакции конденсации с очередной молекулой ацетил-КоА 9. Напишите реакцию субстратного фосфорилирования в цикле трикарбоновых кислот, назовите фермент. Дайте определения понятия «субстратное фосфорилирование» и укажите его биологическое значение. Субстратное фосфорилирование— синтез АТФ, не связанный с электронтранспортной системой, при котором остаток фосфорной кислоты (Н2РО3) переносится на АДФ от высокоэнергетического (фосфорилированного) соединения. Субстратное фосфорилирование на уровне сукцинил-КоА, в ходе которого энергия, освобождающаяся при гидролизе тиоэфирной связи, запасается в форме молекулы ГТФ. В отличие от окислительного фосфорилирования, этот процесс протекает без образования электрохимического потенциала митохондриальной мембраны
Напишите реакции цикла Кребса, в которых образуется СО2. Назовите ферменты и коферменты.
Напишите формулы и названия субстратов НАД-зависимых ферментов в цикле Кребса. Приведите названия ферментов. Укажите дальнейшую судьбу НАДН2.
В цикле Кребса происходит дегидрирование (окисление) субстратов (изоцитрат, α-кетоглутарат, малат). В результате этих реакций образуются НАДН. Эта восстановленная форма кофермента окисляется в митохондриальной дыхательной цепи сопряжённо с синтезом АТФ из АДФ и Н3РО4.
Укажите последовательность и приведите названия компонентов митохондриальной дыхательной цепи. Дайте определение понятия «окислительное фосфорилирование». Укажите локализацию процесса окислительного фосфорилирования в клетке. Ферментные комплексы дыхательной цепи (обозначены участки сопряжения окисления и фосфорилирования): I. НАДН-KoQ-редуктаза (содержит промежуточные акцепторы водорода: флавинмононуклеотид и железосерные белки). II. Сукцинат-KoQ-редуктаза (содержит промежуточные акцепторы водорода: ФАД и железосерные белки). III. KoQН2-цитохром с-редуктаза (содержит акцепторы электронов: цитохромы b и с1, железосерные белки). IV. Цитохром с-оксидаза (содержит акцепторы электронов: цитохромы а и а3, ионы меди Cu2+). В качестве промежуточных переносчиков электронов выступают убихинон (коэнзим Q) и цитохром с. Окислительное фосфорилирование - окисление НАДН и ФАДН2, протекающее сопряжённо с синтезом АТФ из АДФ и Н3РО4. Локализация ферментов дыхательной цепи – внутренняя митохондриальная мембрана. 13. Дайте определение понятия «протонный трансмембранный потенциал». Опишите процесс его образования (локализация, источник энергии, белки, участвующие в его создании). Укажите пути использования протонного трансмембранного потенциала в митохондриях. Протонный трансмембранный потенциал (ΔµН+) – это состояние, при котором наружная поверхность внутренней мембраны приобретает положительный заряд, а внутренняя – отрицательный, т.е. создаётся градиент концентрации протонов с более кислым значением рН снаружи. Ферментные комплексы дыхательной цепи (обозначены участки сопряжения окисления и фосфорилирования): I. НАДН-KoQ-редуктаза (содержит промежуточные акцепторы водорода: флавинмононуклеотид и железосерные белки). II. Сукцинат-KoQ-редуктаза (содержит промежуточные акцепторы водорода: ФАД и железосерные белки). III. KoQН2-цитохром с-редуктаза (содержит акцепторы электронов: цитохромы b и с1, железосерные белки). IV. Цитохром с-оксидаза (содержит акцепторы электронов: цитохромы а и а3, ионы меди Cu2+).
Компоненты дыхательной цепи, расположенные во внутренней митохондриальной мембране, в ходе переноса электронов могут «захватывать» протоны из матрикса митохондрий и передавать их в межмембранное пространство, образую трансмембранный потенциал. Энергия протонного трансмембранного потенциала используется для: 2.Энергия переноса электронов используется для выработки тепла. 14. Охарактеризуйте роль Н+-зависимой АТФ-азы. Укажите локализацию и источник энергии для работы Н+-зависимой АТФ-азы.Укажите биологическую роль АТФ в клетке. Компоненты дыхательной цепи, расположенные во внутренней митохондриальной мембране, в ходе переноса электронов могут «захватывать» протоны из матрикса митохондрий и передавать их в межмембранное пространство. Протоны, выведенные в межмембранное пространство за счёт энергии переноса электронов, снова переходят в митохондриальный матрикс. Этот процесс осуществляется ферментом Н+-зависимой АТФ-азой. Фермент состоит из двух частей (см. рисунок 9.4): водорастворимой каталитической части (F1) и погружённого в мембрану протонного канала (F0). Переход ионов Н+ из области с более высокой в область с более низкой их концентрацией сопровождается выделением свободной энергии, за счёт которой синтезируется АТФ.
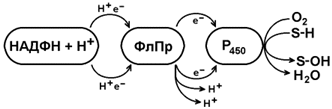
Энергия, аккумулированная в форме АТФ, используется в организме для обеспечения разнообразных биохимических и физиологических процессов. Запомните основные примеры использования энергии АТФ: 1) синтез сложных химических веществ из более простых (реакции анаболизма); 2) сокращение мышц (механическая работа); 3) образование трансмембранных биопотенциалов; 4) активный транспорт веществ через биологические мембраны. Дайте определение понятия «микросомальное окисление». Представьте в виде схемы цепь переноса электронов от НАДФН к кислороду при микросомальном окислении. Укажите локализацию процесса, субстратную специфичность и биологическую роль. Микросомальное окисление является одним из этапов биотрансформации – обезвреживания неполярных (нерастворимых в воде) соединений как эндогенного происхождения, так и чужеродных для организма веществ (ксенобиотиков).
Она представляет собой короткую цепь переноса водорода и включает несколько последовательно расположенных в мембране ЭПС белков-ферментов. Источником электронов и протонов в этой цепи является восстановленный кофермент НАДФН, который образуется в реакциях пентозофосфатного пути окисления глюкозы. Промежуточным акцептором Н+ и е— служит флавопротеин (ФлПр), содержащий кофермент ФАД. Конечное звено в цепи микросомального окисления - цитохром Р450. Это - сложный белок, хромопротеин, в качестве простетической группы содержит гем. Цитохром Р450 является монооксигеназой, то есть ферментом, включающим один из атомов молекулярного кислорода в окисляемое вещество. Поэтому цепь реакций микросомального окисления называют также монооксигеназной цепью. В результате окисления субстратов повышается их растворимость в воде, скорость выведения из организма. Биотрансформация лекарственных веществ, как правило, снижает их токсичность.
16. Дайте определение понятия «углеводы». Приведите примеры. Охарактеризуйте биологическую роль углеводов в организме человека. Углеводы - полигидроксикарбонильные соединения и их производные, Их характерным признаком является наличие альдегидной (-СН=О) или кетонной (>C=O) групп и не менее 2 гидроксильных (-ОН) групп. Функции углеводов. Углеводы выполняют в организме следующие функции: 1. Энергетическая. Углеводы служат источником энергии. За счет их окисления удовлетворяется примерно половина всей потребности человека в энергии. При окислении 1 г углеводов выделяется около 16,9 кДж энергии. 2. Резервная. Крахмал и гликоген представляют собой форму хранения питательных веществ, выполняя функцию временного депо глюкозы. 3. Структурная. Целлюлоза и другие полисахариды растений образуют прочный остов; в комплексе с белками и липидами они входят в состав биомембран всех клеток. 4. Защитная. Кислые гетерополисахариды (гиалуроновая и хондроитинсерная кислоты) выполняют роль биологического смазочного материала, выстилая трущиеся поверхности суставов, слизистой пищеварительных путей, носа, бронхов, трахеи и др. 5. Антикоагулянтная. Гепарин обладает важными биологическими свойствами, в частности препятствует свёртыванию крови. 6. Углеводы являются источником углерода, который необходим для синтеза белков, нуклеиновых кислот, липидов и других соединений. 17. Дайте определение понятия «гомополисахариды». Приведите примеры. Представьте в виде схемы стадии катаболизма крахмала. Укажите биологическую роль пищевого крахмала и гликогена для человека. Гомополисахарид – это полисахарид, который состоит из одинаковых моносахаридных остатков (крахмал, гликоген, целлюлоза, декстран). Гидролиз крахмала начинается в ротовой полости. В слюне содержится фермент амилаза, частично расщепляющая крахмал. Основное место переваривания крахмала - тонкий кишечник. Туда поступает амилаза сока поджелудочной железы. Продуктом действия амилазы является мальтоза. Мальтоза далее расщепляется с помощью мальтазы до глюкозы. Глюкоза поглощается из крови клетками всех тканей и органов. Крахмал и гликоген представляют собой форму хранения питательных веществ, выполняя функцию временного депо глюкозы. Углеводы служат источником энергии 18. Дайте определение понятия «гетерополисахариды». Приведите примеры веществ этой группы углеводов. Укажите их функции в организме.
Гетерополисахарид - это полисахарид, который состоит из разных моносахаридных остатков (гиалуроновая кислота, хондроитинсерная кислота, гепарин). Углеводы служат источником энергии Гиалуроновая кислота связывает воду в межклеточных пространствах, повышая тем самым сопротивление тканей сжатию. Одна молекула гиалуроновой кислоты связывает и удерживает около себя до 500 молекул воды. Она участвует в транспорте и распределении воды в тканях. Гиалуроновая кислота определяет барьерную и защитную функции межклеточного пространства. Внутри суставов она действует как смазка суставных поверхностей, внутри глаза способствует нормализации внутриглазного давления. Хондроитинсерные кислоты - участвуют в водно-солевом обмене, в регулировании клеточного деления, обладают антикоагулирующим действием. Гепарин обладает важными биологическими свойствами, в частности препятствует свёртыванию крови. 19. Дайте определение понятия «дисахариды». Приведите примеры, укажите названия мономеров, которые входят в их состав. Назовите ферменты, участвующие в I стадии катаболизма дисахаридов. Дисахариды - углеводы, содержащие 2 моносахаридных остатка, соединенных, при помощи гликозидных связей - лактоза, сахароза, мальтоза. Мальтоза расщепляется с помощью мальтазы до глюкозы, дисахарид лактоза (содержащаяся в молоке) расщепляется с помощью лактазы до глюкозы и галактозы. Дисахарид сахароза (содержащаяся в пищевом сахаре) расщепляется с помощью сахаразы до глюкозы и фруктозы.
|
||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 1980; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.201.186 (0.016 с.) |