Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
П'ятичленні гетероцикли з одним гетероатомом
Пірол Фуран Тіофен
П'ятичленні гетероцикли можна розглядати, як продукт заміщення в бензеновому ядрі фтагмента —СН=СН— на гетероатом з неподіленою парою електронів. ρ-Обіталь гетероатома, на якій розташована неподілена пара електронів вступає у спряження з π-орбіталями двох π-зв’язків, утворюючи циклічну спряжену π-електронну систему, у якій на 5-ти спряжених орбіталях знаходяться 6 електронів (4 р-електрони від двох подвійних зв'язків і два від гетероатома). Така циклічна спряжена система відповідає правилу Хюккеля, а значить має ароматичний характер. Вказані гетероцикли мають досить високу енергію резонансної стабілізації, хоч і меншу, ніж у бензену. Так, енергія спряження для тіофону складає приблизно 120 кДж/моль, піролу 110, а для фурану – 80 кДж/моль. Нагадаємо, що енергія спряження бензену становить 152 кДж/моль. Зрозуміло, що середня електронна густина в їх молекулах вища, ніж в молекулі бензену, і кожен атом циклу несе частковий негативний заряд. Причому, на α-атомах вуглецю він більший, ніж на β. (δ- > δ′-).
Цікаво відмітити, що в результаті спряження електронної пари азоту пірол втрачає основні властивості, притаманні іншим амінам. З тієї ж причини фуран не проявляє властивостей етерів, а тіофен – сульфідів. Так, останній не окиснюється за атомом сірки, що характерно для аліфатитчних сульфідів. Розглянемо окремі п’ятичленні гетероцикли. Фуран та його похідні Фуран - безбарвна рідина із запахом хлороформу. Одержання Основний промисловий метод добування фурану - декарбонілування фурфуролу
Фурфурол Декарбоксилювання2-фуранкарбонової (пірослизової) кислоти
Фурфурол і пірослизову кислоту одержують, відповідно, з альдопентоз і цукрової кислоти.
Альдопентоза Фурфурол
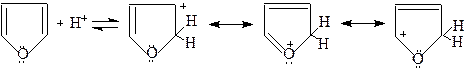
Цукрова 2-Фуранкарбонова кислота (пірослизова) кислота Хімічні властивості Ацидофобні властивості Фуран під дією кислот легко протонується за α-вуглецевим атомом, втрачаючи при цьому ароматичні властивості. Утворений спряжений катіон далі обсмолюється або полімеризується з розривом циклу. Таке руйнування структури під дією кислот називається ацидофобністю.
При введенні у фурановий цикл електроноакцепторних замісників стійкість гетероциклу до дії кислот підвищується.
Реакції електрофільного заміщення Як уже зазначалось, у α,α′-положеннях фурану спостерігається підвищена електронна густина. Тому в реакціях SE утворюються переважно α-похідні. Цьому також сприяє більша стабільність проміжного σ-комплексу (А), завдяки більш вираженому спряженню, порівняно з комплексом (В)
Незважаючи на низьку стабільність, фуран здатний до реакцій електрофільного заміщення (сульфування, нітрування, ацилювання, галогенування), хоча умови цих реакцій сильно відрізняються від тих, у яких реагує бензен. Це пов’язано, в першу чергу, з високою ацидофобністю фурану. 2.2.1. Галогенування Безпосередня взаємодія з бромом може призвести до окиснення фурану, тому як бромуючий агент використовують комплекс піридину або діоксану з бромом.
2.2.2. Нітрування Фуран можна пронітрувати ацетилнітратом у присутності піридину.
Сульфування Комплекс піридину з сірка(VI)оксидом є доволі активним сульфуючим агентом, здатним сульфувати фуран.
2.2.4. Ацилювання фурану здійснюють у присутності кислот Льюїса (ZnCI2 або SnCI4 . Як ацилюючі агенти, використовують, переважно, ангідриди кислот.
Реакції приєднання При каталітичному гідруванні фуран перетворюється у тетрагідрофуран
Тетрагідрофуран
Реакції дієнового синтезу Фуран може реагувати як 1,3-дієн, тобто, виявляє проміжні властивості між ароматичними і дієновими сполуками.
Малеїновий ангідрид Ангідрид 3,6-ендоксо- 1,2,3,6--тетрагідрофталевої кислоти
Реакція окиснення При окисненні фурану отримують малеїновий ангідрид.
Тіофен та його похідні Тіофен є найстійкішим із п'ятичленних гетероциклів. Він не має ацидофобних властивостей (не боїться кислот). Підвищена стабільність тіофену пояснюється здатністю атома сірки надавати вакантні d-орбіталі для делокалізації π-електронів, а також великим атомним радіусом атома сірки, завдяки чому утворюється цикл з меншими викривленнями валентних кутів, а значить і з меншим напруженням циклу.
Одержання Тіофен виділяють із кам'яновугільної смоли або синтезують із бутану і сірки
При взаємодії ацетилену з сірководнем також утворюється тіофен.
Хімічні властивості
|
||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 677; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.128.206.48 (0.014 с.) |